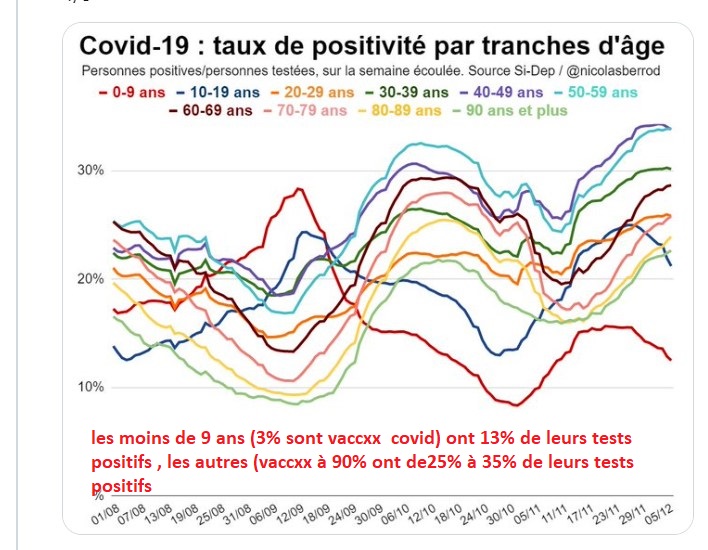
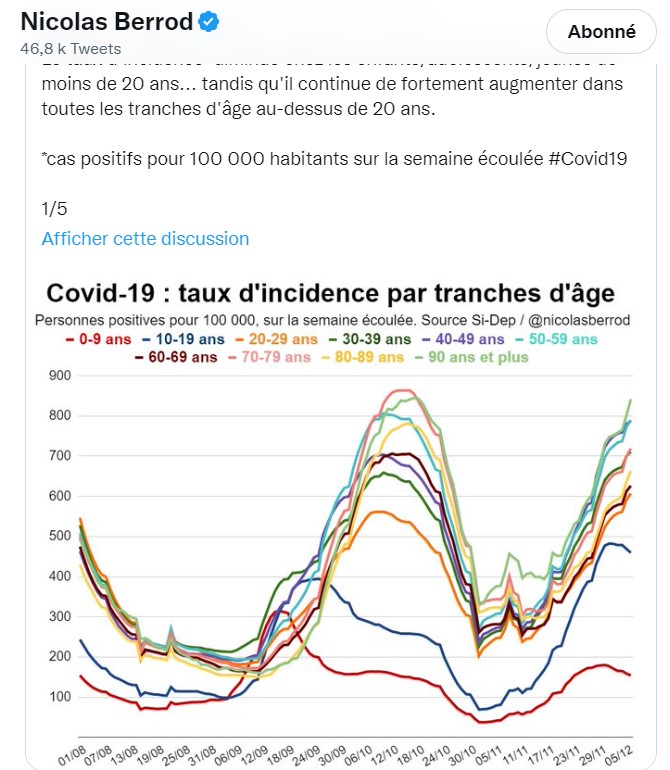
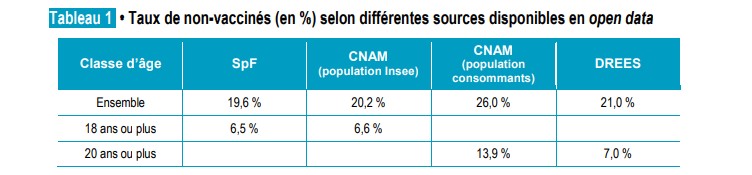
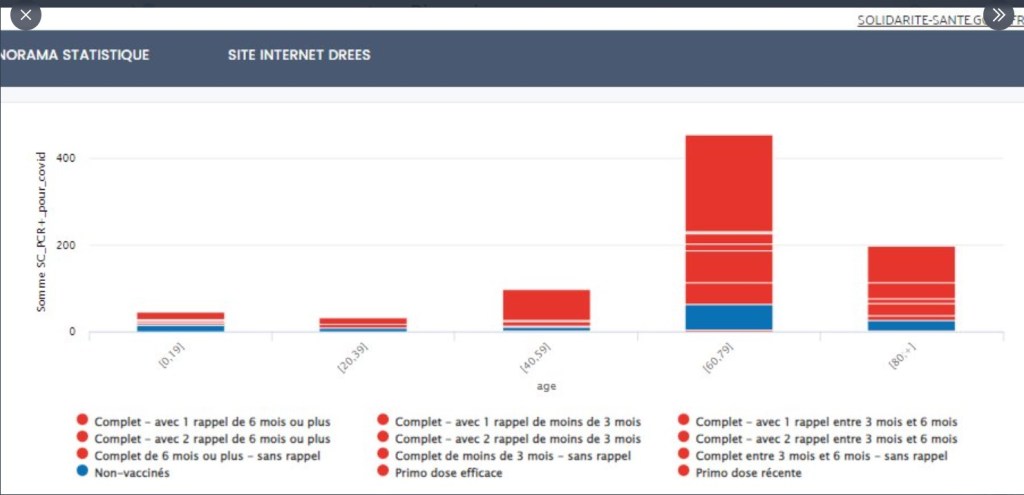
Un mois de censure sur Facebook et surtout la radiation de Linkedin pour un simple post ? merci de m’aider en vous abonnant au blog et en diffusant massivement cette lettre ouverte à la directrice France de Linkedin et si vous le pouvez en lui écrivant
En me censurant, en détruisant mon compte vous assumez donc avec certitude ,devant l’histoire ,les malades, leurs proches que les vaccins covid n’ont pas de conséquences sur les maladies à prions.

Lettre ouverte à Madame Fabienne Arata, directrice générale de LinkedIn France
le 13 /12/2022
Référence
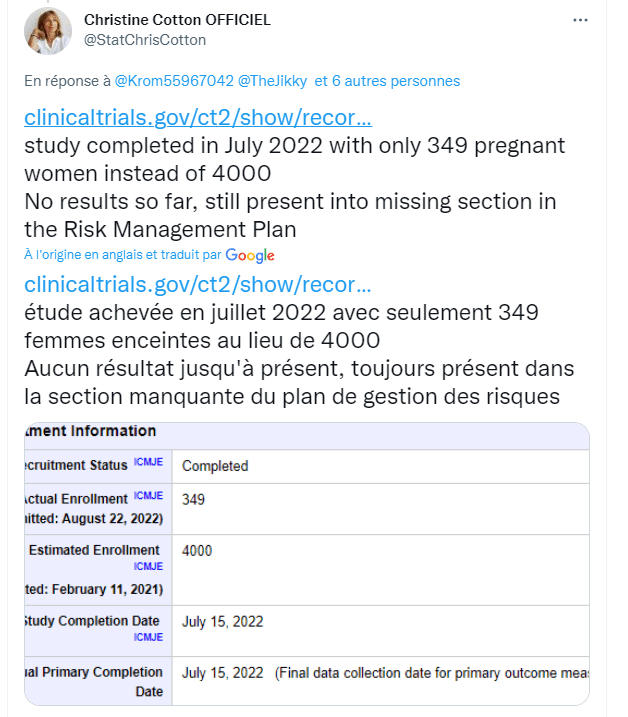
Vous avez pris la décision de supprimer mon compte Linkedin ouvert en 2013. Cette décision serait liée à la publication d’un post de quelques lignes renvoyant à un article de mon blog intitulé ; « le dernier avertissement de Luc Montagnier ».
Cet article faisait le compte rendu des derniers articles du Prix Nobel mais également de quatre études très récentes publiées par des scientifiques de renommée mondiale posant clairement la question des risques entre Arm et prions .
Ces études se réfèrent elles-mêmes à plusieurs centaines d’autres publications.
Dans un passé récent la connaissance par un plus large public d’études scientifiques a contribué à mettre fin à de nombreux scandales sanitaires . Depuis trois ans la diffusion d’études scientifiques a contribué à une meilleure prise en charge de la covid en brisant de fausses informations largement répandues par la presse dite main stream.
Ainsi : l’importance de la prise en charge précoce des malades, le rôle des anti inflammatoires et des anticoagulants. Encore , l’abandon de l’intubation au profit de l’oxygène à haute pression , la reconnaissance du rôle de la vitamine D .
De même de nombreux pays ont pris conscience des effets secondaires des vaccinations ce qui a conduit à les remettre en cause pour les plus jeunes.
De nouvelles études trop peu connues mettent en évidence les risques mortels de confusion entre covid et paludisme . Soigner avec du doliprane quelqu’un qui fait une crise grave de paludisme ne le protègera pas , l’artémisinine l’aurait sauvé….
Ce qui est publié dans des revues scientifiques mais censuré par des « fact chekers » peut sauver des vies.
La responsabilité y compris pénale de ceux qui censurent sera engagée
En me censurant, en détruisant mon compte vous assumez donc avec certitude ,devant l’histoire et les malades, que les vaccins covid n’ont pas de conséquences sur les maladies à prions.
Le libre accès aux publications scientifiques est la seule arme disponible pour les lanceurs d’alerte face aux conflits d’intérêts .
Je vous demande donc de restaurer mon compte
Je vous prie de croire à l’expression de mes sentiments distingués
Patrice Gibertie
Universitaire retraité
Les dernières publications du Nobel Luc Montagnier , avec JC Perez
Worse Than the Disease? Reviewing Some Possible Unintended Consequences of the mRNA Vaccines Against COVID-19
https://zenodo.org/record/7304759#.Y4oKGXbMK3A
I ere étude
Dans « Innate Immune Suppression by SARS-CoV-2 mRNA Vaccinations: The Role of G-quadruplexes, Exosomes and MicroRNAs », Stephanie Seneff, Ph.D., and Drs. Peter McCullough, Greg Nigh et Anthony Kyriakopoulos expliquent comment les injections de COVID-19 suppriment votre fonction immunitaire innée et comment elles peuvent provoquer des maladies neurologiques.
Stephanie Seneff, Ph.D. , , » Innate Immune Suppression by SARS-CoV-2 mRNA Vaccinations: The Role of G-quadruplexes, Exosomes and MicroRNAs « , publié dans le numéro de juin de Food and Chemical Toxicologie.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9012513/
2eme étude
Prion-like Domains in Spike Protein of SARS-CoV-2 Differ across Its Variants and Enable Changes in Affinity to ACE2
https://pubmed.ncbi.nlm.nih.gov/35208734/
Nous passons ensuite en revue les deux composants et la réponse biologique prévue à ces vaccins, y compris la production de la protéine de pointe elle-même, et leur relation potentielle avec un large éventail de pathologies induites aiguës et à long terme, telles que les troubles sanguins, les maladies neurodégénératives et les maladies auto-immunes.
3eme étude
https://ijvtpr.com/index.php/IJVTPR/article/view/23
Une autre étude américaine a émis l’hypothèse qu’une protéine de pointe mal repliée pourrait à son tour créer une région de prion mal repliée qui pourrait être capable d’interagir avec des prions sains pour causer des dommages, conduisant à la MCJ.
4eme étude
Une étude évaluée par des pairs en Turquie ( pdf ) en octobre 2021 décrit un premier cas suspect
Creutzfeldt-Jakob Disease After the COVID-19
Vaccination
LES AUTRES ETUDES
- Abe M., Bonini N.M. MicroRNAs and neurodegeneration: role and impact. Trends Cell Biol. 2013;23(1):30–36. doi: 10.1016/j.tcb.2012.08.013. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Agashe D., Martinez-Gomez N.C., Drummond D.A., Marx C.J. Good codons, bad transcript: large reductions in gene expression and fitness arising from synonymous mutations in a key enzyme. Mol. Biol. Evol. 2013;30:549–560. doi: 10.1093/molbev/mss273. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Akiyama H., Kakiuchi S., Rikitake J., Matsuba H., Sekinada D., Kozuki Y., Iwata N. Immune thrombocytopenia associated with Pfizer-BioNTech’s BNT162b2 mRNA COVID-19 vaccine. IDCases. 2021;25 doi: 10.1016/j.idcr.2021.e01245. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Al-Khalaf H.H., Aboussekhra A. p16 controls p53 protein expression through miR-dependent destabilization of MDM2. Mol. Cancer Res. 2018;16(8):1299–1308. doi: 10.1158/1541-7786.MCR-18-0017. [PubMed] [CrossRef] [Google Scholar]
- Alsamman K., El-Masry O.S. Interferon regulatory factor 1 inactivation in human cancer. Biosci. Rep. 2018;38(3) doi: 10.1042/BSR20171672. 2018. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Andries O., Mc Cafferty S., De Smedt S.C., Weiss R., Sanders N.N., Kitada T. N1-methylpseudouridine-incorporated mRNA outperforms pseudouridine-incorporated mRNA by providing enhanced protein expression and reduced immunogenicity in mammalian cell lines and mice. J. Contr. Release. 2015;217:337–344. doi: 10.1016/j.jconrel.2015.08.051. [PubMed] [CrossRef] [Google Scholar]
- Asmana Ningrum R. Human interferon α-2b: a therapeutic protein for cancer treatment. Sci. Tech. Rep. 2014 doi: 10.1155/2014/970315. 2014. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Atoui A., Jarrah K., Al Mahmasani L., Bou‐Fakhredin R., Taher A.T. Deep venous thrombosis and pulmonary embolism after COVID‐19 mRNA vaccination. Ann. Hematol. 2022:1–3. doi: 10.1007/s00277-021-04743-1. [Epub ahead of print] [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Avolio E., Gamez M., Gupta K., Foster R., Berger I., Caputo M., Davidson A., Hill B., Madeddu P. The SARS-CoV-2 spike protein disrupts the cooperative function of human cardiac pericytes – endothelial cells through CD147 receptor-mediated signalling: a potential non-infective mechanism of COVID-19 microvascular disease. bioRxiv preprint. 2020 doi: 10.1101/2020.12.21.423721. December 21. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Babendure J.R., Babendure J.L., Ding J.H., Tsien R.Y. Control of mammalian translation by mRNA structure near caps. RNA. 2006;12(5):851–861. doi: 10.1261/rna.2309906. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Babic T., Browning K.N. The role of vagal neurocircuits in the regulation of nausea and vomiting. Eur. J. Pharmacol. 2014;722:38–47. doi: 10.1016/j.ejphar.2013.08.047. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Bahl K., Senn J.J., Yuzhakov O., Bulychev A., Brito L.A., Hassett K.J., Laska M.E., Smith M., Almarsson Ö., Thompson J., et al. Preclinical and clinical demonstration of immunogenicity by mRNA vaccines against H10N8 and H7N9 influenza viruses. Mol. Ther. 2017;25(6):1316–1327. doi: 10.1016/j.ymthe.2017.03.035. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Bansal S., Perincheri S., Fleming T., Poulson C., Tiffany B., Bremner R.M., Mohanakumar T. Cutting edge: circulating exosomes with COVID spike protein are induced by BNT162b2 (PfizerBioN-Tech) vaccination prior to development of antibodies: a novel mechanism for immune activation by mRNA vaccines. J. Immunol. 2021;207(10):2405–2410. doi: 10.4049/jimmunol.2100637. [PubMed] [CrossRef] [Google Scholar]
- Barone V., Camilli F., Crisci M., Scandellari C., Barboni P., Lugaresia A. Inflammatory optic neuropathy following SARS-CoV-2 mRNA vaccine: description of two cases. J. Neurol. Sci. 2021;429:118186. doi: 10.1016/j.jns.2021.118186. [CrossRef] [Google Scholar]
- Bezzi G., Piga E.J., Binolfi A., Armas P. CNBP binds and unfolds in vitro G-quadruplexes formed in the SARS-CoV-2 positive and negative genome strands. Int. J. Mol. Sci. 2021;22(5):2614. doi: 10.3390/ijms22052614. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Bhurani V., Mohankrishnan A., Morrot A., Dalai S.K. Developing effective vaccines: cues from natural infection. Int. Rev. Immunol. 2018;37(5):249–265. doi: 10.1080/08830185.2018.1471479. [PubMed] [CrossRef] [Google Scholar]
- Bidwell B.N., Slaney C.Y., Withana N.P., Forster S., Cao Y., Loi S., Andrews D., Mikeska T., Mangan N.E., Samarajiwa S.A., et al. Silencing of Irf7 pathways in breast cancer cells promotes bone metastasis through immune escape. Nat. Med. 2012;18(8):1224–1231. doi: 10.1038/nm.2830. [PubMed] [CrossRef] [Google Scholar]
- Blanco-Melo D., Nilsson-Payant B.E., Liu W.C., Uhl S., Hoagland D., Møller R., Jordan T.X., Oishi K., Panis M., Sachs D., et al. Imbalanced host response to SARS-CoV-2 drives development of COVID-19. Cell. 2020;181(5):1036–1045 e9. [PMC free article] [PubMed] [Google Scholar]
- Borbolis F., Syntichaki P. Cytoplasmic mRNA turnover and ageing. Mech. Ageing Dev. 2015;152:32–42. doi: 10.1016/j.mad.2015.09.006. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Brosh-Nissimov T., Orenbuch-Harroch E., Chowers M., Elbaz M., Nesher L., Stein M., Maor Y., Cohen R., Hussein K., Weinberger M., et al. BNT162b2 vaccine breakthrough: clinical characteristics of 152 fully vaccinated hospitalized COVID-19 patients in Israel. Clin. Microbiol. Infect. 2021;27(11):1652–1657. doi: 10.1016/j.cmi.2021.06.036. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Buckley N.E., Hosey A.M., Gorski J.J., Purcell J.W., Mulligan J.M., Harkin D.P., Mullan P.B. BRCA1 regulates IFN-γ signaling through a mechanism involving the type I IFNs. Mol. Cancer Res. 2007;5(3):261–270. doi: 10.1158/1541-7786.MCR-06-0250. [PubMed] [CrossRef] [Google Scholar]
- Cancer risk and BRCA1 gene mutations. 2021. https://www.facingourrisk.org/info/hereditary-cancer-and-genetic-testing/hereditary-cancer-genes-and-risk/genes-by-name/brca1/cancer-risk Available at:
- Centers for Disease Control and Prevention . 2021. Coronavirus Disease 2019 (COVID-19)https://www.cdc.gov/coronavirus/2019-ncov/science/science-briefs/vaccine-induced-immunity.html#anchor_1635540449320 [online] Available at: [Google Scholar]
- Centers for Disease Control and Prevention . 2021. COVID-19 Booster Shot.https://www.cdc.gov/coronavirus/2019-ncov/vaccines/booster-shot.html [online] Available at: [Google Scholar]
- Chahar H.S., Bao X., Casola A. Exosomes and their role in the life cycle and pathogenesis of RNA viruses. Viruses. 2015;7:3204–3225. doi: 10.3390/v7062770. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Chan K.L., Peng B., Umar M.I., Chan C.Y., Sahakyan A.B., Le M.T.N., Kwok C.K. Structural analysis reveals the formation and role of RNA G-quadruplex structures in human mature microRNAs. Chem. Commun. 2018;54(77):10878–10881. doi: 10.1039/c8cc04635b. [PubMed] [CrossRef] [Google Scholar]
- Chaudhary N., Weissman D., Whitehead K.A. mRNA vaccines for infectious diseases: principles, delivery and clinical translation. Nat. Rev. Drug Discov. 2021;20:817–838. doi: 10.1038/s41573-021-00283-5. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Chauvineau‐Grenier A., Bastard P., Servajeank A., Gervais A., Rosain J., Jouanguy E., Cobat A., Casanova J.-L., Rossi B. Autoantibodies neutralizing type I interferons in 20% of COVID‐19 deaths in a French hospital. J. Clin. Immunol. 2022;27 doi: 10.1007/s10875-021-01203-3. January. [Epub ahead of print] [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Choi H.S., Lee H.M., Jang Y.-J., Kim C.-H., Ryua C.J. Heterogeneous nuclear ribonucleoprotein A2/B1 regulates the self-renewal and pluripotency of human embryonic stem cells via the control of the G1/S transition. Stem Cell. 2013;31:2647–2658. doi: 10.1002/stem.1366. [PubMed] [CrossRef] [Google Scholar]
- Choi Y.E., Pan Y., Park E., Konstantinopoulos P., De S., D’Andrea A., Chowdhury D. MicroRNAs downregulate homologous recombination in the G1 phase of cycling cells to maintain genomic stability. Elife. 2014;3 doi: 10.7554/eLife.02445. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Choi S., Lee S., Seo J.-W., Kim M.-J., Jeon Y.H., Park J.H., Lee J.K., Yeo N.S. Myocarditis-induced sudden death after BNT162b2 mRNA COVID-19 vaccination in korea: case report focusing on histopathological findings. J. Kor. Med. Sci. 2021;36(40):e286. doi: 10.3346/jkms.2021.36.e286. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Cines D.B., Bussel J.B. SARS-CoV-2 vaccine-induced immune thrombotic thrombocytopenia. N. Engl. J. Med. 2021;384:2254–2256. doi: 10.1056/NEJMe2106315. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Collier D.A., De Marco A., Ferreira I.A.T.M., Meng B., Datir R.P., Walls A.C., et al. Sensitivity of SARS-CoV-2 B.1.1.7 to mRNA vaccine-elicited antibodies. Nature. 2021;593:136–141. doi: 10.1038/s41586-021-03412-7. [PubMed] [CrossRef] [Google Scholar]
- Consoli S., Dono F., Evangelista G., D’Apolito M., Travaglini D., Onofrj M., Bonanni L. Status migrainosus: a potential adverse reaction to Comirnaty (BNT162b2, BioNtech/Pfizer) COVID-19 vaccinea case report. Neurol. Sci. 2021;22:1–4. doi: 10.1007/s10072-021-05741-x. [Epub ahead of print] Nov. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Créange A. A role for interferon-beta in Guillain-Barré Syndrome? BioDrugs. 2000;14(1):1–11. doi: 10.2165/00063030-200014010-00001. [PubMed] [CrossRef] [Google Scholar]
- Crow A.R., Lazarus A.H. Role of Fcgamma receptors in the pathogenesis and treatment of idiopathic thrombocytopenic purpura. J. Pediatr. Hematol. Oncol. 2003;25(Suppl. 1):S14S18. doi: 10.1097/00043426-200312001-00004. [PubMed] [CrossRef] [Google Scholar]
- Danese E., Montagnana M., Salvagno G.L., Peserico D., Pighi L., De Nitto S., Henry B.M., Porru S., Lippi G. Comprehensive assessment of humoral response after Pfizer BNT162b2 mRNA Covid-19 vaccination: a three-case series. Clin. Chem. Lab. Med. 2021;59(9):1585–1591. doi: 10.1515/cclm-2021-0339. [PubMed] [CrossRef] [Google Scholar]
- De Andrea M., Ravera R., Gioia D., Gariglio M., Landolfo S. The interferon system: an overview. Eur. J. Paediatr. Neurol. 2002;6:A41–A46. doi: 10.1053/ejpn.2002.0573. [PubMed] [CrossRef] [Google Scholar]
- de Beuckelaer A., Pollard C., Van Lint S., Roose K., Van Hoecke L.V., Naessens T., Udhayakumar V.K., Smet M., Sanders N., Lienenklaus S., et al. Type I interferons interfere with the capacity of mRNA lipoplex vaccines to elicit cytolytic T cell responses. Mol. Ther. 2016;24(11):2012–2020. doi: 10.1038/mt.2016.161. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- de Gonzalo-Calvo D., Benítez I.D., Pinilla L., Carratalá A., Moncusí-Moix A., Gort-Paniello C., Molinero M., González J., Torres G., Bernal M., et al. Circulating microRNA profiles predict the severity of COVID-19 in hospitalized patients. Transl. Res. 2021;236:147–159. doi: 10.1016/j.trsl.2021.05.004. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- De Paolis V., Lorefice E., Orecchini E., Carissimi C., Laudadio I., Fulci V. Epitranscriptomics: a new layer of microRNA regulation in cancer. Cancers. 2021;13(13):3372. doi: 10.3390/cancers13133372. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Decker C.J., Parker R. P-bodies and stress granules: possible roles in the control of translation and mRNA degradation. Cold Spring Harbor Perspect. Biol. 2012;4(9):a012286. doi: 10.1101/cshperspect.a012286. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Delannoy A.S., Hober D., Bouzidi A., Wattre P. Role of interferon alpha (IFN‐α) and interferon gamma (IFN‐γ) in the control of the infection of monocyte‐like cells with Human Cytomegalovirus (HCMV) Microbiol. Immunol. 1999;43(12):1087–1096. [PubMed] [Google Scholar]
- Dodick D., Silberstein S. Central sensitization theory of migraine: clinical implications. Headache. 2006;46(Suppl. 4):S18291. doi: 10.1111/j.1526-4610.2006.00602.x. [PubMed] [CrossRef] [Google Scholar]
- Doulberis M., Papaefthymiou A., Kotronis G., Gialamprinou D., Soteriades E.S., Kyriakopoulos A., et al. Does COVID-19 vaccination warrant the classical principle « ofelein i mi vlaptin. Medicina (Kaunas). 2021;57(3):253. doi: 10.3390/medicina57030253. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Dumortiera J. Liver injury after mRNA-based SARS-CoV-2 vaccination in a liver transplant recipient. Clin. Res. Hepatol. Gastroenterol. 2022;46 doi: 10.1016/j.clinre.2021.101743. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Dunn G.P., Bruce A.T., Sheehan K.C.F., Shankaran V., Uppaluri R., Bui J.D., Diamond M.S., Koebel C.M., Arthur C., White J.M., et al. A critical function for type I interferons in cancer immunoediting. Nat. Immunol. 2005;6(7):722–729. doi: 10.1038/ni1213. [PubMed] [CrossRef] [Google Scholar]
- Erb H.H., Langlechner R.V., Moser P.L., Handle F., Casneuf T., Verstraeten K., Schlick B., Schäfer G., Hall B., Sasser K., Culig Z., Santer F.R., et al. IL6 sensitizes prostate cancer to the antiproliferative effect of IFNα2 through IRF9. Endocr. Relat. Cancer. 2013;20(5):677. doi: 10.1530/ERC-13-0222. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Erman A.B., Kejner A.E., Norman B.S., Hogikyan D., Feldman E.L. Disorders of cranial nerves IX and X. Semin. Neurol. 2009;29(1):8592. doi: 10.1055/s-0028-1124027. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Eviston T., Croxson G.R., Kennedy P.G.E., Hadlock T., Krishnan A.V. Bell’s palsy: aetiology, clinical features and multidisciplinary care. J. Neurol. Neurosurg. Psychiatry. 2015;86 doi: 10.1136/jnnp-2014-309563. [PubMed] [CrossRef] [Google Scholar]
- Farazi T.A., Hoell J.I., Morozov P., Tuschl T. MicroRNAs in human cancer. Adv. Exp. Med. Biol. 2013;774:1–20. doi: 10.1007/978-94-007-5590-1_1. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Fathy R.A., McMahon D.E., Lee C., Chamberlin G.C., Rosenbach M., Lipoff J.B., Tyagi A., Desai S.R., French L.E., Lim H.W., et al. Varicella-zoster and herpes simplex virus reactivation post-COVID-19 vaccination: a review of 40 cases in an International Dermatology Registry. JEADV. 2022;36(1):e6–e9. doi: 10.1111/jdv.17646. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Fay M.M., Lyons S.M., Ivanov P. RNA G-quadruplexes in biology: principles and molecular mechanisms. J. Mol. Biol. 2017;429(14):2127–2147. doi: 10.1016/j.jmb.2017.05.017. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- FDA . Vaccines and Related Biological Products Advisory Committee December 10, 2020 Meeting Announcement. 2021. https://www.fda.gov/advisory-committees/advisory-committee-calendar/vaccines-and-related-biological-products-advisory-committee-december-10-2020-meeting- announcement [Google Scholar]
- FDA . Vaccines and Related Biological Products Advisory Committee December 17, 2020 Meeting Announcement. 2021. https://www.fda.gov/advisory-committees/advisory-committee-calendar/vaccines-and-related-biological-products-advisory-committee-december-17-2020-meeting-announcement [Google Scholar]
- Feng B., Eknoyan G., Guo Z.S., Jadoul M., Rao H.Y., Zhang W., Wei L. Effect of interferon- alpha-based antiviral therapy on hepatitis C virus-associated glomerulonephritis: a meta-analysis. Nephrol. Dial. Transplant. 2012;27(2):640–646. [PubMed] [Google Scholar]
- Fenton A.M., Hammill S.C., Rea R.F., Low P.A., Shen W.-K. Vasovagal syncope. Ann. Intern. Med. 2000;133(9):714–725. doi: 10.7326/0003-4819-133-9-200011070-00014. [PubMed] [CrossRef] [Google Scholar]
- Finnberg N.K., El-Deiry W.S. TRAIL death receptors as tumor suppressors and drug targets. Cell Cycle. 2008;7(11):1525–1528. doi: 10.4161/cc.7.11.5975. [PubMed] [CrossRef] [Google Scholar]
- Forni G., Mantovani A. COVID-19 Commission of Accademia Nazionale dei Lincei, Rome. COVID-19 vaccines: where we stand and challenges ahead. Cell Death Differ. 2021;28(2):626–639. doi: 10.1038/s41418-020-00720-9. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Garg A., Seeliger B., Derda A.A., Xiao K., Gietz A., Scherf K., Sonnenschein K., Pink I., Hoeper M.M., Welte T., et al. Circulating cardiovascular microRNAs in critically ill COVID-19 patients. Eur. J. Heart Fail. 2021;23(3):468–475. doi: 10.1002/ejhf.2096. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Gavras I., Gavras H. Angiotensin II as a cardiovascular risk factor. J. Hum. Hypertens. 2002;16(Suppl. 2):S2–S6. doi: 10.1038/sj.jhh.1001392. [PubMed] [CrossRef] [Google Scholar]
- Girardi T., De Keersmaecker K. T-ALL: ALL a matter of translation? Haematologica. 2015;100(3):293–295. doi: 10.3324/haematol.2014.118562. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Goldman S., Bron D., Tousseyn T., Vierasu I., Dewispelaere L., Heimann P., Cogan E., Goldman M. Rapid progression of angioimmunoblastic T cell lymphoma following BNT162b2 mRNA vaccine booster shot: a case report. Front. Med. 2021;8 doi: 10.3389/fmed.2021.798095. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Gordon D.E., Hiatt J., Bouhaddou M., Rezelj V.V., Ulferts S., Braberg H., et al. Comparative host-coronavirus protein interaction networks reveal pan-viral disease mechanisms. Science. 2020;370(6521) doi: 10.1126/science.abe9403. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Gould F.D.H., Lammers A.R., Mayer C.J., German R.Z. Specific vagus nerve lesion have distinctive physiologic mechanisms of dysphagia. Front. Neurol. 2019;10:1301. doi: 10.3389/fneur.2019.01301. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Guo X., Namekata K., Kimura A., Harada C., Harada T. The renin-angiotensin system regulates neurodegeneration in a mouse model of optic neuritis. Am. J. Pathol. 2017;187(12):2876–2885. doi: 10.1016/j.ajpath.2017.08.012. [PubMed] [CrossRef] [Google Scholar]
- Hadjadj J., Yatim N., Barnabei L., Corneau A., Boussier J., Smith N., Péré H., Charbit B., Bondet V., Chenevier-Gobeaux C., et al. Impaired type I interferon activity and inflammatory responses in severe COVID-19 patients. Science. 2020;369(6504):718–724. doi: 10.1016/j.cell.2020.04.026. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Han S.H., Choe J. Diverse molecular functions of m6A mRNA modification in cancer. Exp. Mol. Med. 2020;52(5):738–749. doi: 10.1038/s12276-020-0432-y. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Heise R., Amann P.M., Ensslen S., Marquardt Y., Czaja K., Joussen S., Beer D., Abele R., Plewnia G., Tampé R., et al. Interferon alpha signaling and its relevance for the upregulatory effect of transporter proteins associated with antigen processing (TAP) in patients with malignant melanoma. PLoS One. 2016;11(1) doi: 10.1371/journal.pone.0146325. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Herdy B., Mayer C., Varshney D., Marsico G., Murat P., Taylor C., D’Santos C., Tannahill D., Balasubramanian S. Analysis of NRAS RNA G-quadruplex binding proteins reveals DDX3X as a novel interactor of cellular G-quadruplex containing transcripts. Nucleic Acids Res. 2018;46(21):11592–11604. doi: 10.1093/nar/gky861. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Hoagland D.A., Møller R., Uhl S.A., Oishi K., Frere J., Golynker T., Horiuchi S., Panis M., Blanco-Melo D., Sachs D., et al. Leveraging the antiviral type I interferon system as a first line of defense against SARS-CoV-2 pathogenicity. Immunity. 2021;54 doi: 10.1016/j.immuni.2021.01.017. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Honda K., Takaoka A., Taniguchi T. Type I interferon [corrected] gene induction by the interferon regulatory factor family of transcription factors. Immunity. 2006;25(3):349–360. doi: 10.1016/j.immuni.2006.08.009. [PubMed] [CrossRef] [Google Scholar]
- Honke K. Biosynthesis and biological function of sulfoglycolipids. Proc. Jpn. Acad. Ser. B Phys. Biol. Sci. 2013;89(4) doi: 10.2183/pjab.89.129. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Hou X., Zaks T., Langer R., Dong Y. Lipid nanoparticles for mRNA delivery. Nat. Rev. Mater. 2021;6:1078–1094. doi: 10.1038/s41578-021-00358-0. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Huang Y., Cai X., Song X., Tang H., Huang Y., Xie S., Hu Y. Steroids for preventing recurrence of acute severe migraine headaches: a meta-analysis. Eur. J. Neurol. 2013;20(8):1184–1190. doi: 10.1111/ene.12155. [PubMed] [CrossRef] [Google Scholar]
- Huang F.T., Sun J., Zhang L., He X., Zhu Y.H., Dong H.J., Wang H.-Y., Zhu L., Zou Huang J.W., et al. Role of SIRT1 in hematologic malignancies. J. Zhejiang Univ. – Sci. B. 2019;20(5):391–398. doi: 10.1631/jzus.B1900148. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Ilyas A.A., Mithen F.A., Dalakas M.C., Wargo M., Chen Z.W., Bielory L., Cook S.D. Antibodies to sulfated glycolipids in Guillain-Barr syndrome. J. Neurol. Sci. 1991;105(1):108–117. doi: 10.1016/0022-510x(91)90126-r. [PubMed] [CrossRef] [Google Scholar]
- Ivanova E.N., Devlin J.C., Buus T.B., Koide A., Cornelius A., Samanovic M.I., Herrera A., Zhang C., Desvignes L., Odum N., Ulrich R., Mulligan M.J., Koide S., Ruggles K.V., Herati R.S., Koralov S.B. Discrete immune response signature to SARS-CoV-2 mRNA vaccination versus infection. medRxiv preprint. 2021 doi: 10.1101/2021.04.20.21255677. April 21. [CrossRef] [Google Scholar]
- Iwanaga J., Fukuoka H., Fukuoka N., Yutori H., Ibaragi S., Tubbs R.S. A narrative review and clinical anatomy of Herpes zoster infection following COVID‐19 vaccination. Clin. Anat. 2021;35(1):45–51. doi: 10.1002/ca.23790. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Jain S.S., Steele J.M., Fonseca B., Huang S., Shah S., Maskatia S.A., Buddhe S., Misra N., Ramachandran P., Gaur L., et al. COVID-19 vaccination–associated myocarditis in adolescents. Pediatrics. 2021;148(5) doi: 10.1542/peds.2021-053427. [PubMed] [CrossRef] [Google Scholar]
- Janeway C.A., Jr., Medzhitov R. Innate immune recognition. Annu. Rev. Immunol. 2002;20:197–216. doi: 10.1146/annurev.immunol.20.083001.084359. [PubMed] [CrossRef] [Google Scholar]
- Jang S.K., Pestova T.V., Hellen C.U.T., Witherell G.W., Wimmer E. Cap-independent translation of picornavirus RNAs: structure and function of the internal ribosomal entry site. Enzyme. 1990;44:292–309. doi: 10.1159/000468766. [PubMed] [CrossRef] [Google Scholar]
- Jaubert C., Bedrat A., Bartolucci L., Di Primo C., Ventura M., Mergny J.-L., Amrane S., Andreola M.-L. RNA synthesis is modulated by G-quadruplex formation in Hepatitis C virus negative RNA strand. Sci. Rep. 2018;8:8120. doi: 10.1038/s41598-018-26582-3. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Jego G.A., Palucka K., Blanck J.-P., Chalouni C., Pascual V., Banchereau J. Plasmacytoid dendritic cells induce plasma cell differentiation through type I interferon and interleukin 6. Immunity. 2003;19 doi: 10.1016/s1074-7613(03)00208-5. [PubMed] [CrossRef] [Google Scholar]
- Jeong M., Ocwieja K.E., Han D., Wackym P.A., Zhang Y., Brown A., Moncada C., Vambutas A., Kanne T., Crain R., et al. Direct SARS-CoV-2 infection of the human inner ear may underlie COVID-19-associated audiovestibular dysfunction. Commun. Med. 2021;1:44. doi: 10.1038/s43856-021-00044-w. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Jhaveri R. The COVID-19 mRNA vaccines and the pandemic: do they represent the beginning of the end or the end of the beginning? Clin. Therapeut. 2021;43(3):549–556. doi: 10.1016/j.clinthera.2021.01.014. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Jiang H., Mei Y.-F. SARS-CoV-2 spike impairs DNA damage repair and inhibits V(D)J recombination in vitro. Viruses. 2021;13(2056) doi: 10.3390/v13102056. [CrossRef] [Google Scholar]
- Kaczmarek R., El Ekiaby M., Hart D.P., Hermans C., Makris M., Noone D., O’Mahony B., Page D., Peyvandi F., Pipe S.W., et al. Vaccination against COVID‐19: rationale, modalities and precautions for patients with haemophilia and other inherited bleeding disorders. Haemophilia. 2021;27(4):515–518. doi: 10.1111/hae.14271. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Kakarougkas A., Ismail A., Klement K., Goodarzi A.A., Conrad S., Freire R., Shibata A., Lobrich M., Jeggo P.A. Opposing roles for 53BP1 during homologous recombination. Nucleic Acids Res. 2013;41(21):9719–9731. doi: 10.1093/nar/gkt729. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Kalra R.S., Kandimalla R. Engaging the spikes: heparan sulfate facilitates SARS-CoV-2 spike protein binding to ACE2 and potentiates viral infection. Signal Transduct. Targeted Ther. 2021;6:39. doi: 10.1038/s41392-021-00470-1. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Kampf G. The epidemiological relevance of the COVID-19-vaccinated population is increasing. Lancet. Reg. Health – Europ. 2021;11 doi: 10.1016/j.lanepe.2021.100272. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Kampf G. The epidemiological relevance of the COVID-19-vaccinated population is increasing. Lancet Reg. Health – Europ. 2021;11 doi: 10.1016/j.lanepe.2021.100272. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Karikó K., Buckstein M., Ni H., Weissman D. Suppression of RNA recognition by toll-like receptors: the impact of nucleoside modification and the evolutionary origin of RNA. Immunity. 2005;23 doi: 10.1016/j.immuni.2005.06.008. [PubMed] [CrossRef] [Google Scholar]
- Katalin Karikó K., Muramatsu H., Welsh F.A., Ludwig J., Kato H., Akira S., Weissman D. Incorporation of pseudouridine into mRNA yields superior nonimmunogenic vector with increased translational capacity and biological stability. Mol. Ther. 2008;16:1833–1840. doi: 10.1038/mt.2008.200. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Katsikas Triantafyllidis K., Giannos P., Mian I.T., Kyrtsonis G., Kechagias K.S. Varicella zoster virus reactivation following COVID-19 vaccination: a systematic review of case reports. Vaccines. 2021;9(9):1013. doi: 10.3390/vaccines9091013. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Kaulen L.D., Doubrovinskaia S., Mooshage C., Jordan B., Purrucker J., Haubner C., Seliger C., Lorenz H.-M., Nagel S., Wildemann B., Bendszus M., Wick W., Schnenberger S. Neurological autoimmune diseases following vaccinations against SARS-CoV-2: a case series. Eur. J. Neurol. 2021:1–9. doi: 10.1111/ene.15147. [Epub ahead of print] [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Kaur A., Fang C.M. An overview of the human immune system and the role of interferon regulatory factors (IRFs) Prog. Microb. Mol. Biol. 2020;3(1) doi: 10.36877/pmmb.a0000129. 2020. [CrossRef] [Google Scholar]
- Kelton J.G., Arnold D.M., Nazy I. Lessons from vaccine-induced immune thrombotic thrombocytopenia. Nat. Rev. Immunol. 2021;21(12):753–755. doi: 10.1038/s41577-021-00642-8. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Khayat-Khoei M., Bhattacharyya S., Katz J., Harrison D., Tauhid S., Bruso P., Houtchens M.K., Edwards K.R., Bakshi R. COVID-19 mRNA vaccination leading to CNS inflammation: a case series. J. Neurol. 2021 Sep 4:1–14. doi: 10.1007/s00415-021-10780-7. [Epub ahead of print] [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Kimura T., Nakajima T., Kamijo Y., Tanaka N., Wang L., Hara A., Sugiyama E., Tanaka E., Gonzalez F.J., Aoyama T. Hepatic cerebroside sulfotransferase is induced by PPAR activation in mice. PPAR Res. 2012 doi: 10.1155/2012/174932. 2012. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Knuckles P., Bühler M. Adenosine methylation as a molecular imprint defining the fate of RNA. FEBS Lett. 2018;592(17):2845–2859. doi: 10.1002/1873-3468.13107. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Kolumam G.A., Thomas S., Thompson L.J., Sprent J., Murali-Krishna K. Type I interferons act directly on CD8 T cells to allow clonal expansion and memory formation in response to viral infection. J. Exp. Med. 2005;202(5) doi: 10.1084/jem.20050821. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Koo J.W., Russo S.J., Ferguson D., Nestler E.J., Duman R.S. Nuclear factor-kappaB is a critical mediator of stress-impaired neurogenesis and depressive behavior. Proc. Natl. Acad. Sci. U. S. A. 2010;107(6):2669–2674. doi: 10.1073/pnas.0910658107. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Kothandan V.K., Kothandan S., Kim D.H., Byun Y., Lee Y.-K., Park I.-K., Hwang S.R. Crosstalk between stress granules, exosomes, tumour antigens, and immune cells: significance for cancer immunity. Vaccines. 2020;8(2):172. doi: 10.3390/vaccines8020172. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Kudla G., Lipinski L., Caffin F., Helwak A., Zylicz M. High guanine and cytosine content increases mRNA levels in mammalian cells. PLoS Biol. 2006;4(6) doi: 10.1371/journal.pbio.0040180. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Kuwahara M., Kusunoki S. Mechanism and spectrum of anti-glycolipid antibody-mediated chronic inflammatory demyelinating polyneuropathy. Clin. Exper. Neuroimmunol. 2018;9(1):65–74. doi: 10.1111/cen3.12452. [CrossRef] [Google Scholar]
- Kwok H.F. Review of COVID-19 vaccine clinical trials — A puzzle with missing pieces. Int. J. Biol. Sci. 2021;7(6):1461. [PMC free article] [PubMed] [Google Scholar]
- Kyriakopoulos A.M., McCullough P.A. Synthetic mRNAs; their analogue caps and contribution to disease. Diseases. 2021;9(3):57. doi: 10.3390/diseases9030057. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Lanz T.V., Ding Z., Ho P.P., Luo J., Agrawal A.N., Srinagesh H., Axtell R., Zhang H., Platten M., Wyss-Coray T., Steinman L. Angiotensin II sustains brain inflammation in mice via TGF-beta. J. Clin. Invest. 2010;120(8):2782–2794. doi: 10.1172/JCI41709. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Lazarus R., Klompas M., Bernstein S. 2010. Electronic Support for Public Health–Vaccine Adverse Event Reporting System (ESP: VAERS). Grant. Final Report, Grant ID: R18 HS; p. 17045. [Google Scholar]
- Lee E.-J., Cines D.B., Gernsheimer T., Kessler C., Michel M., Tarantino M.D., Semple J.W., Arnold D.M., Godeau B., Lambert M.P., Bussel J.B. Thrombocytopenia following pfizer and Moderna SARS-CoV-2 vaccination. Am. J. Hematol. 2021;96(5):534–537. [PMC free article] [PubMed] [Google Scholar]
- Lemberger T., Staels B., Saladin R., Desvergne B., Auwerx J., Wahli W. Regulation of the peroxisome proliferator-activated receptor alpha gene by glucocorticoids. J. Biol. Chem. 1994;269(40):24527–24530. doi: 10.1093/toxsci/kfn260. [PubMed] [CrossRef] [Google Scholar]
- Lensen R., Netea M.G., Rosendaal F.R. Hepatitis C virus reactivation following COVID-19 vaccination — A case report. Int. Med. Case Rep. J. 2021;14:573–575. doi: 10.2147/IMCRJ.S328482. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Letarov A.V., Babenko V.V., Kulikov E.E. Free SARS-CoV-2 spike protein S1 particles may play a role in the pathogenesis of COVID-19 infection. Biochemistry (Mosc.) 2021;86(3):257–261. doi: 10.1134/S0006297921030032. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Leung D.W., Amarasinghe G.K. When your cap matters: structural insights into self vs non-self recognition of 5′ RNA by immunomodulatory host proteins. Curr. Opin. Struct. Biol. 2016;36:133–141. doi: 10.1016/j.sbi.2016.02.001. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Li Y., Huang R., Wang L., Hao J., Zhang Q., Ling R., Yun J. Micro RNA‐762 promotes breast cancer cell proliferation and invasion by targeting IRF7 expression. Cell Prolif. 2015;48(6):643–649. doi: 10.1111/cpr.12223. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Lindenmann J. From interference to interferon: a brief historical introduction. Philos. Trans. R. Soc. Lond. B Biol. Sci. 1982;299(1094):3–6. [PubMed] [Google Scholar]
- Liu T., Khanna K.M., Chen X., Fink D.J., Hendricks R.L. CD8(+) T cells can block herpes simplex virus type 1 (HSV-1) reactivation from latency in sensory neurons. J. Exp. Med. 2000;191(9):1459–1466. doi: 10.1084/jem.191.9.1459. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Liu J., Wang J., Xu J., Xia H., Wang Y., Zhang C., Chen W., Zhang H., Liu Q., Zhu R., et al. Comprehensive investigations revealed consistent pathophysiological alterations after vaccination with COVID-19 vaccines. Cell Discov. 2021;7(1):99. doi: 10.1038/s41421-021-00329-3. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Lladó I., Fernández-Bernáldez A., Rodríguez-Jiménez P. Varicella zoster virus reactivation and mRNA vaccines as a trigger. JAAD. Case Rep. 2021;15:62–63. doi: 10.1016/j.jdcr.2021.07.011. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Lu Y., Harada M., Kamijo Y., Nakajima T., Tanaka N., Sugiyama E., Kyogashima M., Gonzalez F.J., Aoyama T. Peroxisome proliferator-activated receptor attenuates high-cholesterol diet-induced toxicity and pro-thrombotic effects in mice. Arch. Toxicol. 2019;93(1) doi: 10.1007/s00204-018-2335-4. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- MacFarlane M., Kohlhaas S.L., Sutcliffe M.J., Dyer M.J., Cohen G.M. TRAIL receptor-selective mutants signal to apoptosis via TRAIL-R1 in primary lymphoid malignancies. Cancer Res. 2005;65(24):11265–11270. doi: 10.1158/0008-5472.CAN-05-2801. [PubMed] [CrossRef] [Google Scholar]
- Maleki A. COVID-19 recombinant mRNA vaccines and serious ocular inflammatory side effects: real or coincidence? J. Ophthalmic Vis. Res. 2021;16(3) doi: 10.18502/jovr.v16i3.9443. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Mann R., Sekhon S., Sekhon S. Drug-induced liver injury after COVID-19 vaccine. Cureus. 2021;13(7) doi: 10.7759/cureus.16491. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Marcus J., Honigbaum S., Shroff S., Honke K., Rosenbluth J., Dupree J.L. Sulfatide is essential for the maintenance of CNS myelin and axon structure. Glia. 2006;53(4):372–381. doi: 10.1002/glia.20292. [PubMed] [CrossRef] [Google Scholar]
- Martini P.G.V., Guey L.T. A new era for rare genetic diseases: messenger RNA therapy. Hum. Gene Ther. 2019;30(10):1180–1189. doi: 10.1089/hum.2019.090. [PubMed] [CrossRef] [Google Scholar]
- Matsuoka M., Tani K., Asano S. Interferon-alpha-induced G1 phase arrest through upregulated expression of CDK inhibitors, p19Ink4D and p21Cip1 in mouse macrophages. Oncogene. 1998;16:2075–2086. doi: 10.1038/sj.onc.1201745. [PubMed] [CrossRef] [Google Scholar]
- Mauro V.P., Chappell S.A. A critical analysis of codon optimization in human therapeutics. Trends Mol. Med. 2014;20(11):604–613. doi: 10.1016/j.molmed.2014.09.003. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- McCarthy C., Carrea A., Diambra L. Bicodon bias can determine the role of synonymous SNPs in human diseases. BMC Genom. 2017;18(1):227. doi: 10.1186/s12864-017-3609-6. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- McKenzie S.E., Taylor S.M., Malladi P., Yuhan H., Cassel D.L., Chien P., Schwartz E., Schreiber A.D., Surrey S., Reilly M.P. The role of the human Fc receptor FcRIIA in the immune clearance of platelets: a transgenic mouse model. J. Immunol. 1999;162:4311–4318. http://www.jimmunol.org/content/162/7/4311 [PubMed] [Google Scholar]
- McKernan K., Kyriakopoulos A.M., McCullough P.A. Differences in vaccine and SARS-CoV-2 replication derived mRNA: implications for cell biology and future disease. OSF Prepr. 2021 doi: 10.31219/osf.io/bcsa6. November 26. [CrossRef] [Google Scholar]
- McLachlan S., Osman M., Dube K., Chiketero P., Choi Y., Fenton N. Analysis of COVID-19 vaccine death reports from the vaccine adverse events reporting system (VAERS) database. Preprint. 2021 doi: 10.13140/RG.2.2.26987.26402. [CrossRef] [Google Scholar]
- Meyer K.D., Patil D.P., Zhou J., Zinoviev A., Skabkin M.A., Elemento O., Pestova T.V., Qian S.-B., Jaffrey S.R. 5′ UTR m(6)A promotes cap-independent translation. Cell. 2015;163(4):999–1010. doi: 10.1016/j.cell.2015.10.012. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Mishra R., Banerjea A.C. SARS-CoV-2 Spike targets USP33-IRF9 axis via exosomal miR-148a to activate human microglia. Front. Immunol. 2021;12 doi: 10.3389/fimmu.2021.656700. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Mittal M.K., Chaudhuri G. Abstracts: First AACR International Conference on Frontiers in Basic Cancer Research–Oct 8–11, 2009. Boston, MA. 2009. https://cancerres.aacrjournals.org/content/69/23_Supplement/A16.short [Google Scholar]
- Mulligan M.J., Lyke K.E., Kitchin N., Absalon J., Gurtman A., Lockhart S., Neuzil K., Raabe V., Bailey R., Swanson K.A., Li P., Koury K., Kalina W., Cooper D., Fontes-Garfias C., Shi P.-Y., Türeci Ö., Tompkins K.R., Walsh E.E., Frenck R., Falsey A.R., Dormitzer P.R., Gruber W.C., Şahin U., Jansen K.U. Phase I/II study of COVID-19 RNA vaccine BNT162b1 in adults. Nature. 2020;586(7830):589–593. doi: 10.1038/s41586-020-2639-4. [PubMed] [CrossRef] [Google Scholar]
- Mungoven T.J., Meylakh N., Marciszewski K.K., Macefield V.G., Macey P.M., Henderson L.A. Microstructural changes in the trigeminal nerve of patients with episodic migraine assessed using magnetic resonance imaging. J. Headache Pain. 2020;21:59. doi: 10.1186/s10194-020-01126-1. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Musella M., Manic G., de Maria R., Vitale I., Sistigue A. Type-I-interferons in infection and cancer: unanticipated dynamics with therapeutic implications. OncoImmunology. 2017;6(5) doi: 10.1080/2162402X.2017.1314424. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Nandha R., Singh H. Renin angiotensin system: a novel target for migraine prophylaxis. Indian J. Pharmacol. 2012;44(2) doi: 10.4103/0253-7613.93840. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- National Cancer Institute BRCA gene mutations: cancer risk and genetic testing fact sheet. 2021. https://www.cancer.gov/about-cancer/causes-prevention/genetics/brca-fact-sheet#what-other-cancers-are-linked-to-harmful-variants-in-brca1-and-brca2 [online] Available at:
- Nevzorova T.A., Mordakhanova E.R., Daminova A.G., Ponomareva A.A., Andrianova I.A., Minh G.L., Rauova L., Litvinov R.L., Weisel J.W. Platelet factor 4-containing immune complexes induce platelet activation followed by calpain-dependent platelet death. Cell Death Dis. 2019;5:106. doi: 10.1038/s41420-019-0188-0. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Olsthoorn R.C. G-quadruplexes within prion mRNA: the missing link in prion disease? Nucleic Acids Res. 2014;42:9327–9333. doi: 10.1093/nar/gku559. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Orlandini von Niessen A.G., Poleganov M.A., Rechner C., Plaschke A., Kranz L.M., Fesser S., Diken M., Löwer M., Vallazza B., Beissert T., et al. Improving mRNA-based therapeutic gene delivery by expression-augmenting 3’ UTRs identified by cellular library screening. Mol. Ther. 2019;27(4):824–836. doi: 10.1016/j.ymthe.2018.12.011. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Otsuka H., Fukao A., Funakami Y., Duncan K.E., Fujiwara T. Emerging evidence of translational control by AU-rich element-binding proteins. Front. Genet. 2019;10:332. doi: 10.3389/fgene.2019.00332.g. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Oudit G.Y., Kassiri Z., Jiang C., Liu P.P., Poutanen S.M., Penninger J.M., Butany J. SARS coronavirus modulation of myocardial ACE2 expression and inflammation in patients with SARS. Eur. J. Clin. Invest. 2009;39(7) doi: 10.1111/j.1365-2362.2009.02153. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Ozaki T., Nakagawara A. Role of p53 in cell death and human cancers. Cancers. 2011;3(1):994–1013. doi: 10.3390/cancers3010994. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Panier S., Boulton S.J. Double-strand break repair: 53BP1 comes into focus. Nat. Rev. 2014;15:9. doi: 10.1038/nrm3719. [PubMed] [CrossRef] [Google Scholar]
- Pardi N., Hogan M.J., Porter F.W., Weissman D. mRNA vaccines – a new era in vaccinology. Nat. Rev. Drug Discov. 2018;17(4):261–279. doi: 10.1038/nrd.2017.243. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Park J.W., Lagniton P., Liu Y., Xu R.H. mRNA vaccines for COVID-19: what, why and how. Int. J. Biol. Sci. 2021;17(6):1446–1460. doi: 10.7150/ijbs.59233. 2021. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Passariello M., Vetrei C., Amato F., De Lorenzo C. Interactions of spike-RBD of SARS-CoV-2 and platelet factor 4: new insights in the etiopathogenesis of thrombosis. Int. J. Mol. Sci. 2021;22:8562. doi: 10.3390/ijms22168562. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Passegu E., Ernst P.A. IFN-alpha wakes up sleeping hematopoietic stem cells. Nat. Med. 2009;15(6) doi: 10.1038/nm0609-612. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Perricone C., Ceccarelli F., Nesher G., Borella E., Odeh Q., Conti F., Shoenfeld Y., Valesini G. Immune thrombocytopenic purpura (ITP) associated with vaccinations: a review of reported cases. Immunol. Res. 2014;60:226–235. doi: 10.1007/s12026-014-8597-x. [PubMed] [CrossRef] [Google Scholar]
- Psichogiou M., Karabinis A., Poulakou G., Antoniadou A., Kotanidou A., Degiannis D., Pavlopoulou I.D., Chaidaroglou A., Roussos S., Mastrogianni E., et al. Comparative immunogenicity of BNT162b2 mRNA vaccine with natural COVID-19 infection. Vaccines (Basel) 2021;9(9):1017. doi: 10.3390/vaccines9091017. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Psichogiou M., Samarkos M., Mikos N., Hatzakis A. Reactivation of Varicella zoster virus after vaccination for SARS-CoV-2. Vaccines. 2021;9:572. doi: 10.3390/vaccines9060572. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Qiu X.-K., Ma J. Alteration in microRNA-155 level correspond to severity of coronary heart disease. Scand. J. Clin. Lab. Invest. 2018;78(3):219–223. doi: 10.1080/00365513.2018.1435904. [PubMed] [CrossRef] [Google Scholar]
- Qiu S., Palavicini J.P., Wang J., Gonzalez N.S., He S., Dustin E., Zou C., Ding L., Bhattacharjee A., Van Skike C.E., et al. Adult-onset CNS myelin sulfatide deficiency is sufficient to cause Alzheimer’s disease-like neuroinflammation and cognitive impairment. Mol. Neurodegener. 2021;16:64. doi: 10.1186/s13024-021-00488-7. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Röltgen K., Nielsen S.C.A., Silva O., Younes S.F., Zaslavsky M., Costales C., Yang F., Wirz O.F., Solis D., Hoh R.A. Immune imprinting, breadth of variant recognition and germinal center response in human SARS-CoV-2 infection and vaccination. Cell. 2022 doi: 10.1016/j.cell.2022.01.018. Jan 25; S0092-8674(22)00076-9. [Epub ahead of print] [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Rasmussen S.A., Abul-Husn N.S., Casanova J.L., Daly M.J., Rehm H.L., Murray M.F. The intersection of genetics and COVID-19 in 2021: preview of the 2021 Rodney Howell Symposium. Genet. Med. 2021;23(6):1001–1003. doi: 10.1038/s41436-021-01113-0. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Ratajczak M.Z., Ratajczak J. Horizontal transfer of RNA and proteins between cells by extracellular microvesicles: 14 years later. Clin. Transl. Med. 2016;5:7. doi: 10.1186/s40169-016-0087-4. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Rhea E.M., Logsdon A.F., Hanse K.M., Williams L.M., Reed M.J., Baumann K.K., Holden S.J., Raber J., Banks W.A., Erickson M.A. The S1 protein of SARS-CoV-2 crosses the blood-brain barrier in mice. Nat. Neurosci. 2021;24:368–378. doi: 10.1038/s41593-020-00771-8. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Rodrigues Figueiredo R., Aparecida Azevedo A., De Oliveira Penido N. Positive association between tinnitus and arterial hypertension. Front. Neurol. 2016;7:171. doi: 10.3389/fneur.2016.00171. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Rodriguez-Perez A.I., Borrajo A., Rodriguez-Pallares J., Guerra M.J., Labandeira-Garcia J.L. Interaction between NADPH-oxidase and Rho-kinase in angiotensin II-induced microglial activation. Glia. 2015;63:466e482. doi: 10.1002/glia.22765. [PubMed] [CrossRef] [Google Scholar]
- Rose J. Critical appraisal of VAERS pharmacovigilance: is the U.S. vaccine adverse events reporting system (VAERS) a Functioning pharmacovigilance system? Sci. Publ. Health Pol. the Law. 2021;3:100–129. [Google Scholar]
- Rouleau S., Glouzon J.S., Brumwell A., Bisaillon M., Perreault J.P. 3′ UTR G-quadruplexes regulate miRNA binding. RNA. 2017;23(8):1172–1179. doi: 10.1261/rna.060962.117. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Rouleau S.G., Garant J.-M., Balduc F., Bisaillon M., Perreault J.-P. G-Quadruplexes influence pri-microRNA processing. RNA Biol. 2018;15(2):198–206. doi: 10.1080/15476286.2017.1405211. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Rusk N. When microRNAs activate translation. Nat. Methods. 2008;5:122–123. doi: 10.1038/nmeth0208-122a. [CrossRef] [Google Scholar]
- Ruther U., Nunnensiek C., Muller H.A., Bader H., May U., Jipp P. Interferon alpha (IFN alpha 2a) therapy for herpes virus-associated inflammatory bowel disease (ulcerative colitis and Crohn’s disease) Hepato-Gastroenterology. 1998;45(21):691–699. doi: 10.1111/j.1348-0421.1999.tb03365.x. [PubMed] [CrossRef] [Google Scholar]
- Sakai Y., Ohga S., Tonegawa Y., Takada H., Nakao F., Nakayama H., Aoki T., Yamamori S., Hara T. Interferon-alpha therapy for chronic active Epstein-Barr virus infection: potential effect on the development of T- lymphoproliferative disease. J. Pediatr. Hematol. Oncol. 1998;20(4):342–346. [PubMed] [Google Scholar]
- Sayers T.J. Targeting the extrinsic apoptosis signaling pathway for cancer therapy. Cancer Immunol. Immunother. 2011;60(8):1173–1180. doi: 10.1007/s00262-011-1008-4. [PubMed] [CrossRef] [Google Scholar]
- Schmidt N., Lareau C.A., Keshishian H., Ganskih S., Schneider C., Hennig T., Melanson R., Werner S., Wei Y., Zimmer M., et al. The SARS-CoV-2 RNA-protein interactome in infected human cells. Nat. Microbiol. 2021;6(3):339–353. doi: 10.1038/s41564-020-00846-z. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Schneider W.M., Chevillotte M.D., Rice C.M. Interferon-stimulated genes: a complex web of host defenses. Anni. Rev. Immunol. 2014;32:513–545. [PMC free article] [PubMed] [Google Scholar]
- Sekiguchi K., Watanabe N., Miyazaki N., Ishizuchi K., Iba C., Tagashira Y., Uno S., Shibata M., Hasegawa N., Takemura R., et al. Incidence of headache after COVID-19 vaccination in patients with history of headache: a cross-sectional study. Cephalalgia. 2021 doi: 10.1177/03331024211038654. [Epub ahead of print. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Seneff S., Nigh G. Worse than the disease? Reviewing some possible unintended consequences of the mRNA vaccines against COVID-19. IJVTPR. 2021;2(1):38–79. [Google Scholar]
- Shabalina S.A., Spiridonov N.A., Kashina A. Sounds of silence: synonymous nucleotides as a key to biological regulation and complexity. Nucleic Acids Res. 2013;41(4):2073–2094. doi: 10.1093/nar/gks1205. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Shatsky I.N., Terenin I.M., Smirnova V.V., Andreev D.E. Cap-independent translation: what’s in a name? Trends Biochem. Sci. 2018;43(11):882–895. doi: 10.1016/j.tibs.2018.04.011. [PubMed] [CrossRef] [Google Scholar]
- Shaw G., Morse S., Ararat M., Graham F.L. Preferential transformation of human neuronal cells by human adenoviruses and the origin of HEK 293 cells. Faseb. J. 2002;16(8):869–871. doi: 10.1096/fj.01-0995fje. [PubMed] [CrossRef] [Google Scholar]
- Shitrit P., Zuckerman N.S., Mor O., Gottesman B.-S., Chowers M. Nosocomial outbreak caused by the SARS-CoV-2 Delta variant in a highly vaccinated population, Israel, July 2021. Euro Surveill. 2021;26(39) doi: 10.2807/1560-7917.ES.2021.26.39.2100822. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Shrotri M., Navaratnam A.M., Nguyen V., Byrne T., Geismar C., Fragaszy E., Beale S., Fong W.L.E., Patel P., Kovar J., et al. Spike-antibody waning after second dose of BNT162b2 or ChAdOx1. Lancet. 2021;398(10298):385–387. [PMC free article] [PubMed] [Google Scholar]
- Simone A., Herald J., Chen A. Acute myocarditis following COVID-19 mRNA vaccination in adults aged 18 years or older. JAMA Intern. Med. 2021;181(12):1668–1670. doi: 10.1001/jamainternmed.2021.5511. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Small E.M., Olson E.N. Pervasive roles of microRNAs in cardiovascular biology. Nature. 2011;469(7330):336–342. doi: 10.1038/nature09783. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Sola I., Almazán F., Zúñiga S., Enjuanes L. Continuous and discontinuous RNA synthesis in coronaviruses. Ann. Rev. Virol. 2015;2(1):265–288. doi: 10.1146/annurev-virology-100114-055218. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Solis M., Goubau D., Romieu-Mourez R., Genin P., Civas A., Hiscott J. Distinct functions of IRF-3 and IRF-7 in IFN-alpha gene regulation and control of anti-tumor activity in primary macrophages. Biochem. Pharmacol. 2006;72(11):1469–1476. doi: 10.1016/j.bcp.2006.06.002. [PubMed] [CrossRef] [Google Scholar]
- Spiegel J., Adhikari S., Balasubramanian S. The structure and function of DNA G-quadruplexes. Trend. Chem. 2020;2(2):123–136. doi: 10.1016/j.trechm.2019.07.002. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Stertz S., Hale B.G. Interferon system deficiencies exacerbating severe pandemic virus infections. Trends Microbiol. 2021;29(11):973–982. doi: 10.1016/j.tim.2021.03.001. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Suberbielle E., Djukic B., Evans M., Kim D.H., Taneja P., Wang X., Finucane M., Knox J., Ho K., Devidze N., et al. DNA repair factor BRCA1 depletion occurs in Alzheimer brains and impairs cognitive function in mice. Nat. Commun. 2015;6:8897. doi: 10.1038/ncomms9897. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Subramanian, S.V.; Kumar, A. Increases in COVID-19 are unrelated to levels of vaccination across 68 countries and 2947 counties in the United States. Eur. J. Epidemiol. 2021, 1-4. doi: 10.1007/s10654-021-00808-7. [PMC free article] [PubMed]
- Sundstedt A., Celander M., Hedlund G. Combining tumor-targeted superantigens with interferon-alpha results in synergistic anti-tumor effects. Int. Immunopharm. 2008;8(3):442–452. doi: 10.1016/j.intimp.2007.11.006. 2008. [PubMed] [CrossRef] [Google Scholar]
- Svitkin U.V., Herdy B., Costa-Mattioli M., Gingras A.-C., Raught B., Sonenberg N. Eukaryotic translation initiation factor 4E availability controls the switch between cap-dependent and internal ribosomal entry site-mediated translation. Mol. Cell Biol. 2005;25(23):10556–10565. doi: 10.1128/MCB.25.23.10556-10565.2005. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Takaoka A., Tamura T., Taniguchi T. Interferon regulatory factor family of transcription factors and regulation of oncogenesis. Cancer Sci. 2008;99(3):467–478. doi: 10.1111/j.1349-7006.2007.00720. [PubMed] [CrossRef] [Google Scholar]
- Testa U. TRAIL/TRAIL‐R in hematologic malignancies. J. Cell. Biochem. 2010;110(1):21–34. doi: 10.1002/jcb.22549. [PubMed] [CrossRef] [Google Scholar]
- Tetz G., Tetz V. Prion-like domains in spike protein of SARS-CoV-2 differ across its variants and enable changes in affinity to ACE2. Microorganisms. 2022;10:280. doi: 10.3390/microorganisms10020280. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Tian W.-L., Guo R., Wang F., Jiang Z.-X., Tang P., Huang Y.-M., Sun L. The IRF9-SIRT1-P53 axis is involved in the growth of human acute myeloid leukemia. Exp. Cell Res. 2018;365:185–193. doi: 10.1016/j.yexcr.2018.02.036. [PubMed] [CrossRef] [Google Scholar]
- Timmers L.F.S.M., Peixoto J.V., Ducati R.G., Bachega J.F.R., de Mattos Pereira L., Caceres R.A., Majolo F., da Silva G.L., Anton D.B., Dellagostin O.A., Henriques J.A.P., Xavier L.L., Goettert M.I., Laufer S. SARS-CoV-2 mutations in Brazil: from genomics to putative clinicalconditions. Sci. Rep. 2021;11:11998. doi: 10.1038/s41598-021-91585-6. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Tronvik E., Stovner L.J., Helde G., Sand T., Bovim G. Prophylactic treatment of migraine with an angiotensin II receptor-blocker: a randomized controlled trial. JAMA. 2003;289(1):65–69. doi: 10.1001/jama.289.1.65. [PubMed] [CrossRef] [Google Scholar]
- Troya J., Bastard P., Planas-Serra L., Ryan P., Ruiz M., de Carranza M., Torres J., Martnez A., Abel L., Casanova J.-L., Pujol A. Neutralizing autoantibodies to type I IFNs in >10% of patients with severe COVID-19 pneumonia hospitalized in Madrid, Spain. J. Clin. Immunol. 2021;41 doi: 10.1007/s10875-021-01036-0. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Tsuno T., Mejido J., Zhao T., Morrow A., Zoon K.C. IRF9 is a key factor for eliciting the antiproliferative activity of IFN-α J. Immunother. 2009;32(8):803. doi: 10.1097/CJI.0b013e3181ad4092. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Uranaka T., Kashio A., Ueha R., Sato T., Bing H., Ying G., Kinoshita M., Kondo K., Yamasoba T. Expression of ACE2, TMPRSS2, and furin in mouse ear tissue, and the implications for SARS-CoV-2 infection. Laryngoscope. 2021;131(6):E2013–E2017. doi: 10.1002/lary.29324. [PubMed] [CrossRef] [Google Scholar]
- Vaers Home VAERS. https://vaers.hhs.gov/data/dataguide.html n.d.). Retrieved December 5, 2021, from.
- van der Wijst M.G.P., Vazquez S.E., Hartoularos G.C., Bastard P., Grant T., Bueno R.>, Lee D.S., Greenland J.R., Sun Y., Perez R., et al. Type I interferon autoantibodies are associated with systemic immune alterations in patients with COVID-19. Sci. Transl. Med. 2021;13(612) doi: 10.1126/scitranslmed.abh2624. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Van Lint S., Renmans D., Broos K., Dewitte H., Lentacker I., Heirman C., Breckpot K., Thielemans K. The ReNAissanCe of mRNA-based cancer therapy. Expert Rev. Vaccines. 2015;14(2):235–251. doi: 10.1586/14760584.2015.957685. [PubMed] [CrossRef] [Google Scholar]
- Vanderlugt C.L., Miller S.D. Epitope spreading in immune-mediated diseases: implications for immunotherapy. Nat. Rev. Immunol. 2002;2:85–95. doi: 10.1038/nri724. [PubMed] [CrossRef] [Google Scholar]
- Verma A.K., Lavine K.J., Lin C.-Y. Myocarditis after covid-19 mRNA vaccination. NEJM. 2021;385:1332–1334. doi: 10.1056/NEJMc2109975. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Verweij M.C., Wellish M., Whitmer T., Malouli D., Lapel M., Jonjić S., Haas J.G., DeFilippis V.R., Mahalingam R., Früh K. Varicella viruses inhibit interferon-stimulated JAK-STAT signaling through multiple mechanisms. PLoS Pathog. 2015;11(5) doi: 10.1371/journal.ppat.1004901. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Wang X.-A., Zhang R., Jiang D., Deng W., Zhang S., Deng S., Zhong J., Wang T., Zhu L.-H., Yang L., et al. Interferon regulatory factor 9 protects against hepatic insulin resistance and steatosis in male mice. Hepatology. 2013;58(2):603–616. doi: 10.1002/hep.26368. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Wang H., Hu H., Zhang K. Overview of interferon: characteristics, signaling and anti-cancer effect. Arch. Biotechnol. Biomed. 2017;1:1–16. [Google Scholar]
- Wang C., Zhang C., Liu L., A X., Chen B., Li Y., Du J. Macrophage-derived mir-155-containing exosomes suppress fibroblast proliferation and promote fibroblast inflammation during cardiac injury. Mol. Ther. 2017;25(1):192–204. doi: 10.1016/j.ymthe.2016.09.001. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Wang N., Zhan Y., Zhu L., Hou Z., Liu F., Song P., Qiu F., Wang X., Zou X., Wan D., et al. Retrospective multicenter cohort study shows early interferon therapy is associated with favorable clinical responses in COVID-19 patients. Cell Host Microbe. 2020;28(3):455–464. doi: 10.1016/j.chom.2020.07.005. e2. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Wang Y., Nakajima T., Gonzalez F.J., Tanaka N. PPARs as metabolic regulators in the liver: lessons from liver-specific PPAR-null mice. Int. J. Mol. Sci. 2020;21:2061. doi: 10.3390/ijms21062061. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Wang E., Thombre R., Shah Y., Latanich R., Wang J. G-Quadruplexes as pathogenic drivers in neurodegenerative disorders. Nucleic Acids Res. 2021;49(9):4816–4830. doi: 10.1093/nar/gkab164. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Wei H., Chen Q., Lin L., Sha C., Li T., Liu Y., Yin X., Xu Y., Chen L., Gao W., Li Y., Zhu X. Regulation of exosome production and cargo sorting. Int. J. Biol. Sci. 2021;17(1):163–177. doi: 10.7150/ijbs.53671. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Weikert U., Kühl U., Schultheiss H.-P., Rauch U. Platelet activation is increased in patients with cardiomyopathy: myocardial inflammation and platelet reactivity. Platelets. 2002;13(8):487–491. doi: 10.1080/0953710021000057857. [PubMed] [CrossRef] [Google Scholar]
- Weiner J., Lewis D., Maertzdorf J., Mollenkopf H., Bodinham C., Pizzoferro K., Linley C., Greenwood A., Mantovani A., Bottazzi B., Denoel P., Leroux-Roels G., Kester K., Jónsdóttir I., van den Berg R.A., Kaufmann S., Del Giudice G. Characterization of potential biomarkers of reactogenicity of licensed antiviral vaccines: randomized controlled clinical trials conducted by the BIOVACSAFE consortium. Sci. Rep. 2019;9(1):20362. doi: 10.1038/s41598-019-56994-8. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Weldon C., Dacanay J.G., Gokhale V., Boddupally P.V.L., Behm-Ansmant I., Burley G.A., Branlant C., Hurley L.M., Dominguez C., Eperon I.C. Specific G-quadruplex ligands modulate the alternative splicing of Bcl-X. Nucleic Acids Res. 2018;46(2):886–896. doi: 10.1093/nar/gkx1122. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Williams G.D., Gokhale N.S., Snider D.L., Horner S.M. The mRNA cap 2′-O-methyltransferase CMTR1 regulates the expression of certain interferon-stimulated genes. mSphere. 2020;5(3) doi: 10.1128/mSphere.00202-20. e00202-e00220. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Wisnewski A.V., Campillo Luna J., Redlich C.A. Human IgG and IgA responses to COVID-19 mRNA vaccines. PLoS One. 2021;16(6) doi: 10.1371/journal.pone.0249499. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Wrapp D., Wang N., Corbett K.S., Goldsmith J.A., Hsieh C.L., Abiona O., Graham B.S., McLellan J.S. Cryo-EM structure of the 2019-nCoV spike in the prefusion conformation. Science. 2020;367(6483):1260–1263. doi: 10.1126/science.abb2507. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Xia X. Detailed dissection and critical evaluation of the Pfizer/BioNTech and Moderna mRNA vaccines. Vaccines. 2021;9:734. doi: 10.3390/vaccines9070734. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Yahi N., Chahinian H., Fantini J. Infection-enhancing anti-SARS-CoV-2 antibodies recognize both the original Wuhan/D614G strain and Delta variants. A potential risk for mass vaccination? J. Infect. 2021;83(5):607–635. doi: 10.1016/j.jinf.2021.08.010. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Yang C., Hu Y., Zhou B., Bao Y., Li Z., Gong C., Yang H., Wang S., Xiao Y. The role of m6A modification in physiology and disease. Cell Death Dis. 2020;11:960. doi: 10.1038/s41419-020-03143-z. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Yoshikawa F.S., Teixeira F.M., Sato M.N., Oliveira L.M. Delivery of microRNAs by extracellular vesicles in viral infections: could the news be packaged? Cells. 2019;8(6):611. doi: 10.3390/cells8060611. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Yu X., Odenthal M., Fries J.W.U. Exosomes as miRNA carriers: formation–function–future. Int. J. Mol. Sci. 2016;17:2028. doi: 10.3390/ijms17122028. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Zaccara S., Ries R.J., Jaffrey S.R. Reading, writing and erasing mRNA methylation. Nat. Rev. 2019;20:608–624. doi: 10.1038/s41580-019-0168-5. [PubMed] [CrossRef] [Google Scholar]
- Zakaria Z., Sapiai N.A., Izaini Ghani A.R. Cerebral venous sinus thrombosis 2 weeks after the first dose of mRNA SARS‐CoV‐2 vaccine. Acta Neurochir. 2021;163(8):2359–2362. doi: 10.1007/s00701-021-04860-w. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Zhang J., Powell S.N. The role of the BRCA1 tumor suppressor in DNA double-strand break repair. Mol. Cancer Res. 2005;3(10):531–539. doi: 10.1158/1541-7786.MCR-05-0192. [PubMed] [CrossRef] [Google Scholar]
- Zhang W., Luo J., Yang F., Wang Y., Yin Y., Strom A., Gustafsson J.Å., Guan X. BRCA1 inhibits AR-mediated proliferation of breast cancer cells through the activation of SIRT1. Sci. Rep. 2016;6:22034. doi: 10.1038/srep22034. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Zhang R., Xiao K., Gu Y., Liu H., Sun X. Whole genome identification of potential G-quadruplexes and analysis of the G-quadruplex binding domain for SARS-CoV-2. Front. Genet. 2020;11 doi: 10.3389/fgene.2020.587829. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Zhao Y., Chen W., Zhu W., Meng H., Chen J., Zhang J. Overexpression of interferon regulatory factor 7 (IRF7) reduces bone metastasis of prostate cancer cells in mice. Oncol. Res. 2017;25(4):511. doi: 10.3727/096504016X14756226781802. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Zhou M., Guo J., Cha J., Chae M., Chen S., Barral J.M., Sachs M.S., Liu Y. Non-optimal codon usage affects expression, structure and function of clock protein FRQ. Nature. 2013;495(7439):111–115. doi: 10.1038/nature11833. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Zin Tun G.S., Gleeson D., Al-Joudeh A., Dube A. Immune-mediated hepatitis with the Moderna vaccine, no longer a coincidence but confirmed. J. Hepatol. 2021 doi: 10.1016/j.jhep.2021.09.031. Oct 5. [Epub ahead of print] [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Zitvogel L., Galluzzi L., Kepp O., Smyth M.J., Kroemer G. Type I interferons in anticancer immunity. Nat. Rev. Immunol. 2015;15(7):405–414. doi: 10.1038/nri3845. [PubMed] [CrossRef] [Google Scholar]
- Zoll J., Erkens Hulshof S., Lanke K., Verduyn Lunel F., Melchers W.J., Schoondermark-van de Ven E., Roivainen M., Galama J.M., van Kuppeveld F.J. Saffold virus, a human Theiler’s-like cardiovirus, is ubiquitous and causes infection early in life. PLoS Pathog. 2009;5(5) doi: 10.1371/journal.ppat.1000416. [PMC free article] [PubMed] [CrossRef] [Google Scholar]