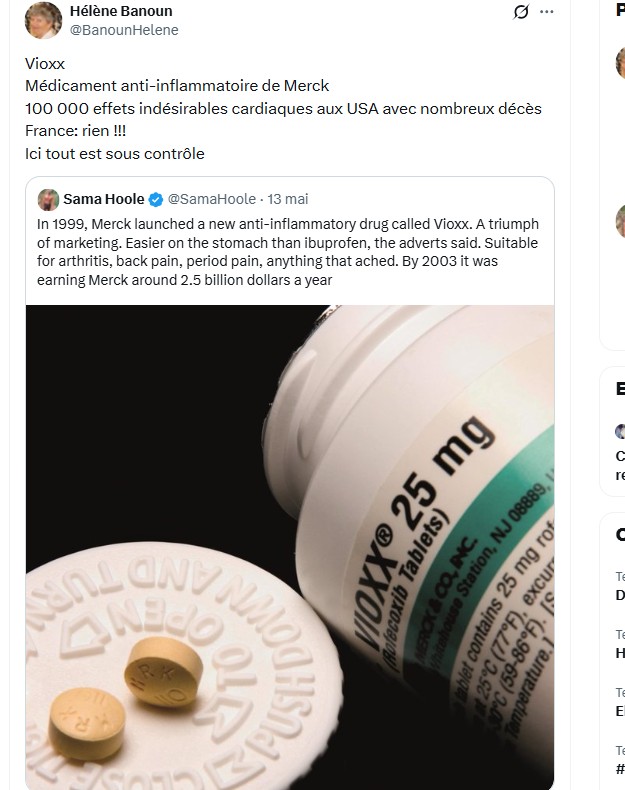
Vioxx (rofecoxib) était bien un anti-inflammatoire (COX-2 sélectif) de Merck, commercialisé de 1999 à 2004. Il a été retiré mondialement en septembre 2004 après la confirmation de risques cardiovasculaires accrus (infarctus, AVC).
en.wikipedia.orgLes chiffres aux États-UnisLes estimations varient selon les sources, mais elles sont élevées :
- Une analyse du Lancet (2004-2005) estime 88 000 à 140 000 cas excédentaires de maladies coronariennes graves aux USA, avec environ 38 000 décès (30-40 % des cas graves). npr.org
- Un analyste de la FDA (David Graham) avait évoqué autour de 27 000 à 55 000 décès potentiels liés au médicament sur la période. pnhp.org
Ces risques augmentaient surtout avec une utilisation prolongée (>18 mois), mais des signaux étaient apparus plus tôt (étude VIGOR en 2000). Merck a été critiqué pour avoir minimisé les données et retardé le retrait. Des milliers de procès ont eu lieu aux USA.
En France
Officiellement, aucun décès n’a été formellement attribué au Vioxx par les autorités sanitaires françaises. Environ 500 000 personnes l’ont pris. Des plaintes et associations de victimes (comme l’AAAVAM) ont signalé des cas suspects (jusqu’à ~250 décès collectés selon certaines sources), mais les expertises judiciaires et les autorités n’ont pas établi de lien causal reconnu dans la majorité des cas.
sante.journaldesfemmes.fr. Statistiquement, proportionnellement à la population et à l’usage, on s’attendrait à des centaines ou milliers de cas graves en France si les risques étaient identiques — mais le système de pharmacovigilance et d’indemnisation (ONIAM, etc.) n’a pas abouti aux mêmes reconnaissances qu’aux USA. Des plaintes pénales ont relancé le sujet vers 2016, sans grand retentissement public comme le Mediator.Pourquoi cette différence ?
- Systèmes différents : Aux USA, les actions de groupe, les jurys et les dommages-intérêts punitifs favorisent plus de reconnaissances et de règlements. En France/Europe, la pharmacovigilance est plus centralisée (ANSM, EMA), avec des seuils de preuve plus stricts pour l’imputabilité individuelle et moins d’incitations financières aux plaintes.
- Sous-déclaration : Les effets indésirables sont souvent sous-notifiés partout, mais particulièrement quand le lien n’est pas évident ou quand le médicament est déjà retiré.
- Vioxx a été approuvé et surveillé des deux côtés de l’Atlantique ; les signaux de risque cardiovasculaire concernaient la classe des coxibs en général.
Le cas Vioxx (comme le Mediator en France) montre que aucun système n’est infaillible : approbation basée sur des essais limités, pression commerciale, signaux tardifs de pharmacovigilance.

Si si sont bien morts ces 10 000 pékins; mais…pas du Vioxx… là est en fait la différence de raisonnement !
Encore un « lapsus » rédactionnel ..?
Mais qui donc rédige les titres de vos article, en particulier ?
J’aimeJ’aime