
Les documents déclassifiés par la justice révèlent des surprises
Le juge Mark T. Pittman (Dallas, Cour d’appel du Texas) vient de récidiver le 9 mai 2023, en exigeant la remise de l’ensemble des données concernant le vaccin pédiatrique Pfizer et le vaccin adulte Moderna, incluant 4,8 millions de pages, sous 2 ans vs les 23,5 que réclamait la FDA. Les laboratoires ont en l’occurrence jusqu’au 31 juin 2025 pour s’exécuter.
La publication de ces données a par ailleurs été jalonnée d’une série d’informations concernant l’origine du virus dont les scientifiques ont acquis la conviction qu’il est issu de recherches de gain de fonction financées clandestinement par le Dr A. Fauci, ancien directeur de l’Institut national des allergies et des maladies infectieuses (NIAID) et ancien conseiller médical de la Maison-Blanche durant la pandémie de COVID-19. On sait également aujourd’hui que la fabrication des vaccins a débuté avant la date officielle, communiquée au public, le PDG de Moderna ayant reconnu dans une interview que sa société avait déjà produit 100 000 doses de vaccin Covid-19 en 2019.
https://twitter.com/odrobsed/status/1632315917286752266?s=20
La divulgation d’un accord de confidentialité montre en réalité que « des candidats vaccins potentiels contre le coronavirus ont été transférés de Moderna à l’Université de Caroline du Nord le 12 décembre 2019, soit dix-neuf jours avant que l’Organisation mondiale de la santé (OMS) n’ait eu connaissance de l’émergence des premiers cas de SARS-CoV-2 à Wuhan » (The Expose).
Un document déclassifié prouve que la production du vaccin Pfizer a commencé en mai 2019
Un lanceur d’alerte pointe aujourd’hui une information inédite, contenue dans un autre document, également déclassifié suite à une requête FOIA, qui permet de répondre à cette question, en tout cas techniquement. Le document en question est le rapport d’évaluation non clinique produit par le régulateur australien (Therapeutic Goods Administration — TGA). La page 40 du rapport montre que la société Acuitas a formulé l’ARNm codant pour la luciférase transmis par BioNTech et référencé (ARN-EH190611-01c) dans le rapport R-20-0072, en trois types de nanoparticules : LNP12 (formulation DODMA:DOPE), LNP5 et LNP8.
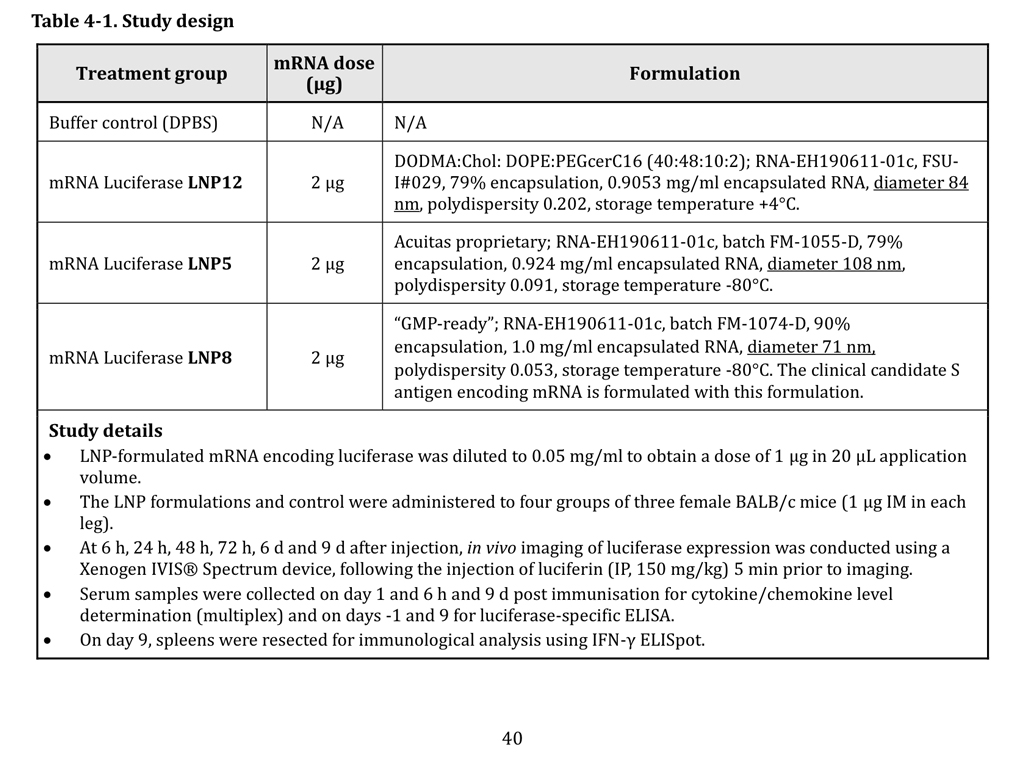
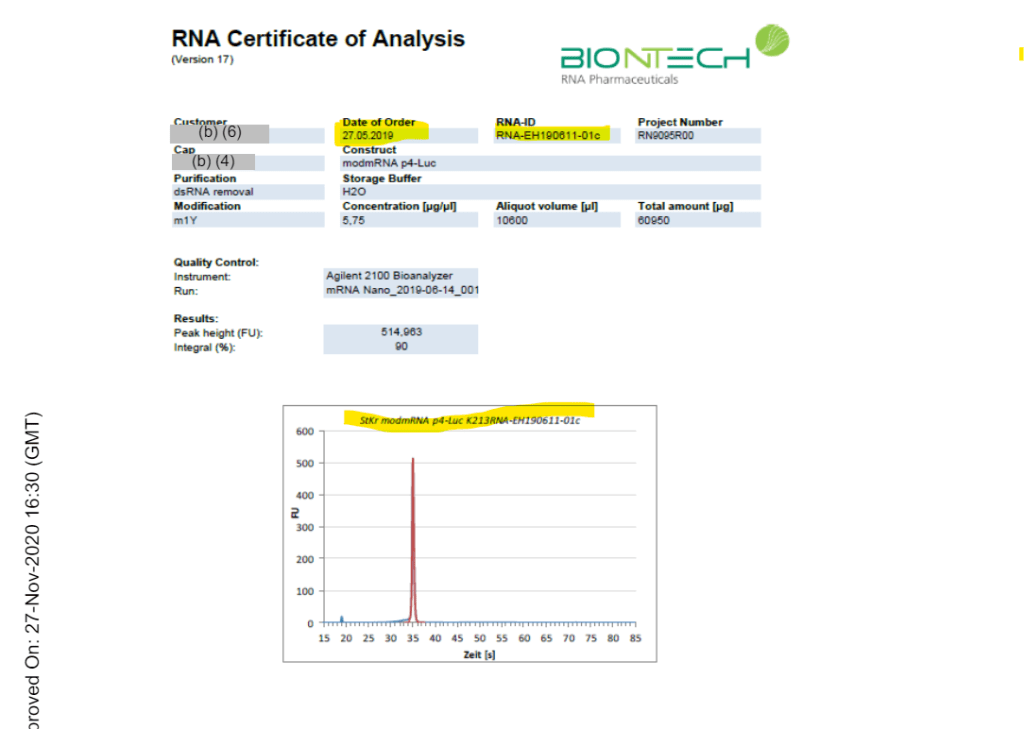
Or la page 29 du rapport BioNTech montre que la formulation des nanoparticules destinées au vaccin (LNP8, comme mentionné à la page 12 du même rapport) a été réalisée le 9 décembre 2019, soit trois semaines avant la divulgation du cas zéro à Wuhan. Les indications de formulation étant strictement identique entre les deux documents, cette concordance ne permet pas de douter que le certificat d’analyse contenu dans le rapport BioNTech concerne les nanoparticules utilisées dans l’étude australienne :
- Référence du produit : RNA-EH190611-01c ;
- No de lot : FM-1074-D ;
- Taux d’encapsulation : 90 % ;
- Concentration en ARN : 1.0 mg/ml ;
- Diamètre : 71 nm ;
- Rendement : 90 %;
- Polydispersité : 0,053 :
- Température de stockage : – 80 °C.
https://modarnlife.substack.com/p/the-pre-2020-bnt162-development-program
https://modarnlife.substack.com
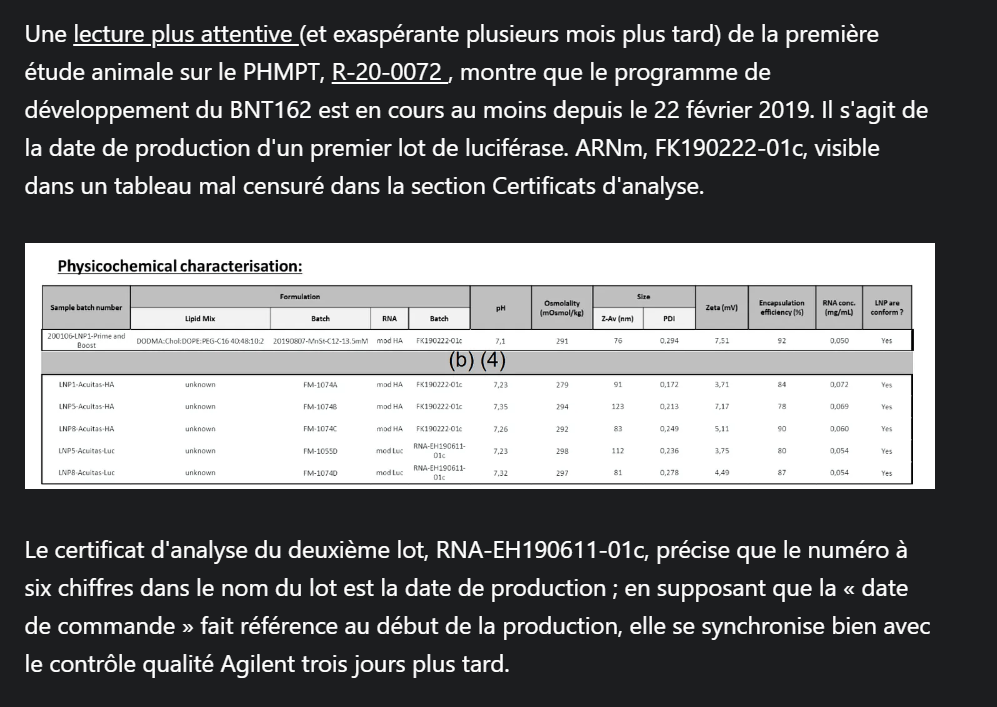



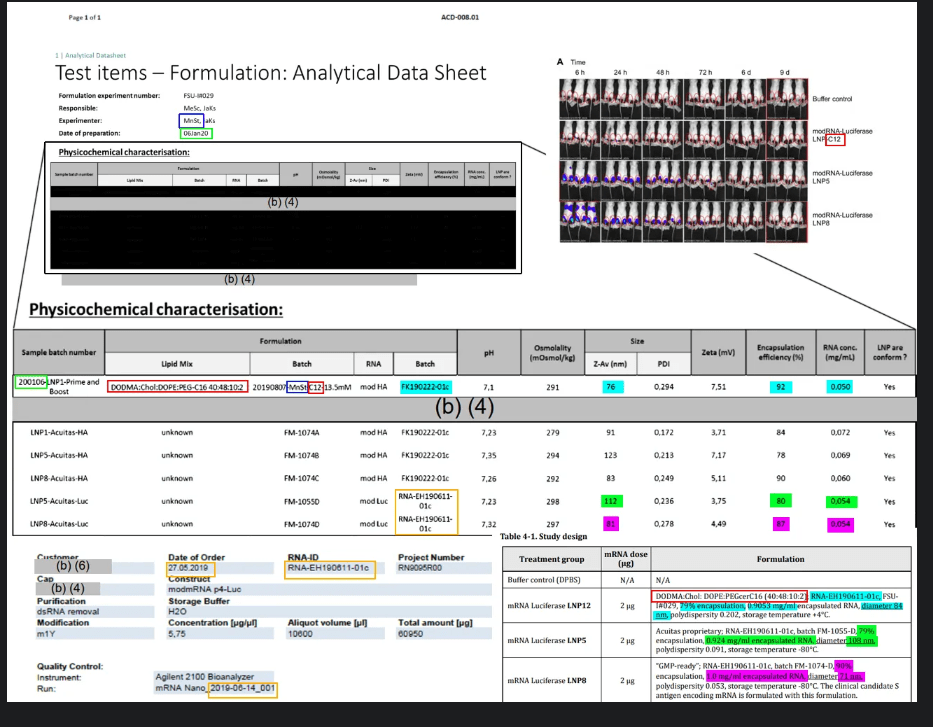
Lorsque vous comparez les zones surlignées en bleu, vert et violet dans les parties TGA et d’étude, vous pouvez voir plusieurs erreurs dans la version TGA : mauvais lot de luciférase et de lipides pour DODMA : DOPE, lots corrects de Luc/lipides pour LNP5/8, aucun. des mesures techniques sont celles rapportées par Acuitas.
Incertain de sa signification, mais remarquable. Hypothétiquement, il pourrait y avoir des différences entre les techniques/appareils/étalonnages de mesure d’Acuitas et de BioNTech, ou le personnel de TGA qui rédige le rapport a mélangé les certificats d’analyse de différentes études. Les autres marquages sont les suivants : la boîte bleue montre que les initiales de l’expérimentateur figurent dans le numéro de lot lipidique pour DODMA:DOPE, renforçant l’idée qu’il s’agissait d’un matériau non Acuitas (en lisant l’étude, ils le disent explicitement, mais tant pis), rouge La boîte montre que DODMA:DOPE était le troisième article testé dans R-20-0072 et que le nom TGA « LNPC12 » pourrait provenir, la boîte orange est le deuxième lot de luciférase.
Chose intéressante, le lot DODMA:DOPE utilisait le FK190222, BioNTech aurait donc dû inclure le certificat d’analyse correspondant de février dans les annexes. D’autres régulateurs ont-ils commis la même « erreur » en attribuant le deuxième lot de luciférase à l’article de test DODMA:DOPE du R-20-0072, dispensant ainsi BioNTech de devoir ajouter un bon de commande d’ARNm de février 2019 plutôt embarrassant au matériel d’étude ? Mai 2019 est déjà assez mauvais, pour être honnête, ce n’est probablement qu’une erreur. Probablement.
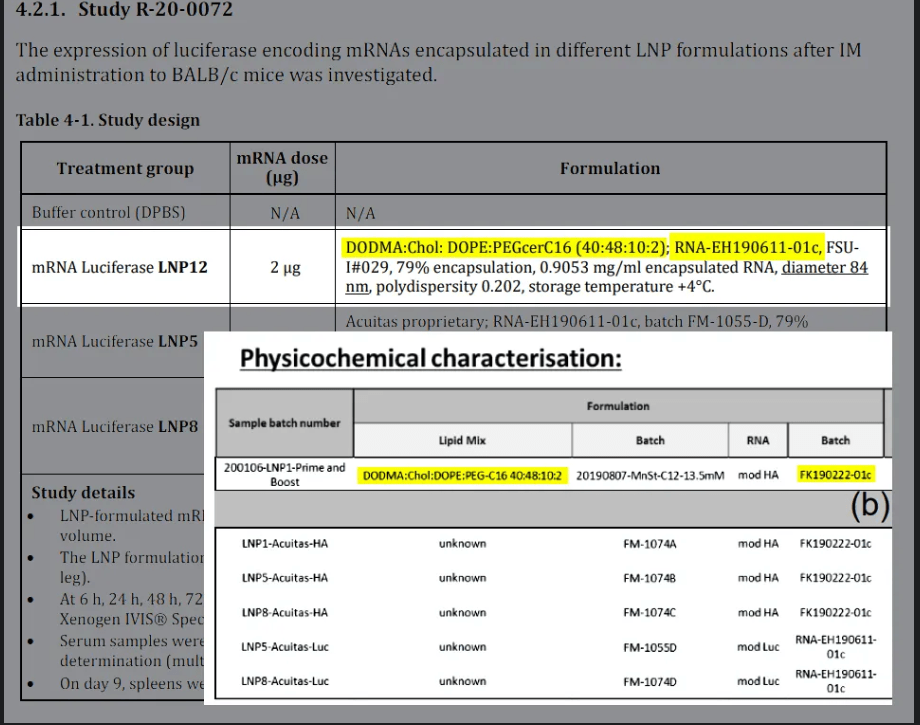
Un autre point d’incertitude était le préfixe FK du premier lot, mais d’autres lots de BioNTech (avant de modifier leur processus de dénomination interne pour ne pas refléter la date d’achèvement) affichent la même structure : deux lettres + six chiffres + caractères superflus. Le deuxième lot de luciférase porte « EH », le premier lot de BNT162b1 porte « KG », etc.
Ce qui reste légèrement nébuleux, c’est la signification du « mod HA » par rapport au « mod Luc ». Le premier code assurément pour la luciférase, comme en témoigne l’imagerie de bioluminescence non censurée dans le rapport TGA.
La transposition des 16 jours entre la date de commande et la date indiquée dans le nom du lot sur le lot FK donne une date de commande du 6 février 2019. Un an plus tard jour pour jour, le patron d’Acuitas, Thomas Madden, serait en Allemagne pour discuter du BNT162-01. essai clinique avec BioNTech et le régulateur allemand Paul-Ehrlich-Institut. Voici un extrait d’une interview PharmaBoardroom de décembre 2020 :

BioNTech s’en était évidemment rendu compte bien avant « lorsque la pandémie a frappé », comme en témoigne la production d’ARNm de luciférase pseudouridylée dès février 2019.
Mon impression : les études formulation pilote + R-20-0072 étaient une pièce maîtresse. BioNTech avait conclu une collaboration en matière de vaccin contre la grippe avec Pfizer en juillet 2018, une couverture parfaite pour commencer à passer du traitement personnalisé du cancer aux maladies infectieuses. Comme en témoigne l’accord du 17 mars 2020 entre Pfizer et BioNTech, Pfizer n’était pas au courant de la R&D d’Acuitas. Ceci est en outre étayé par la première mention d’Acuitas dans les documents déposés par BioNTech auprès de la SEC en 2021, où BioNTech divulgue l’octroi de licences pour la technologie Acuitas. BioNTech était en train de « développer » une plateforme de vaccins contre les maladies infectieuses avec Acuitas au plus bas, dépensant beaucoup d’argent pour cette technologie alors qu’ils sont déjà en partenariat avec la plus grande société pharmaceutique au monde ?
Je dis « en développement » en raison du timing propice : le lot de luciférase FK190222 date de février, EH190611 date de juin, mais la première livraison du produit à BioNTech a eu lieu le 26 novembre. Le prochain bon de livraison n’arrive que quinze jours plus tard. Quinze jours pendant lesquels BioNTech réalise l’étude de formulation pilote, évalue les résultats et Acuitas formule les produits pour le bon de livraison du 11 décembre et l’étude R-20-0072.
Ce n’est pas du développement, c’est une configuration scriptée qui attend d’être mise en œuvre. La visite de la chancelière allemande Angela Merkel à Wuhan en septembre 2019 prend certainement un tout autre jour.
Une citation de l’annexe 1 de la fuite de l’EMA :
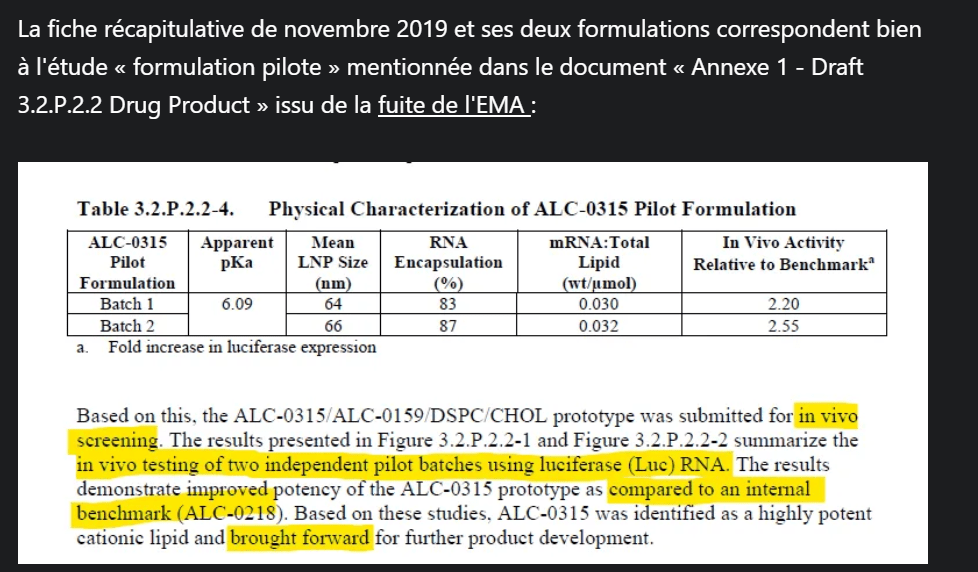
Le développement de la formulation a commencé par le criblage de nanoparticules lipidiques. Cela impliquait l’incorporation des nouveaux lipides dans des LNP encapsulant l’ARN, puis leur soumission à un processus de sélection comprenant une formulation pilote et une caractérisation physique pour déterminer l’adéquation aux tests in vivo et à la détermination de l’activité dans un modèle murin d’expression d’ARN.
Au cours de la formulation pilote, des lipides cationiques candidats ont été formulés avec de l’ARN codant pour la luciférase et d’autres composants lipidiques dans une composition standardisée comprenant le lipide cationique (ALC-0315, ALC-0218, etc.), un lipide PEGylé (ALC-0159), du DSPC. et le cholestérol. L’utilisation de l’ARN codant pour la luciférase a permis une évaluation visuelle de l’expression et de la traduction dans des systèmes modèles. Les résultats de ces études ont conduit à la sélection de l’ALC-0315.
Il est tout simplement terrifiant de voir à quel point tous les organismes de réglementation ont négligé les dates de ces études et développements de recherche.
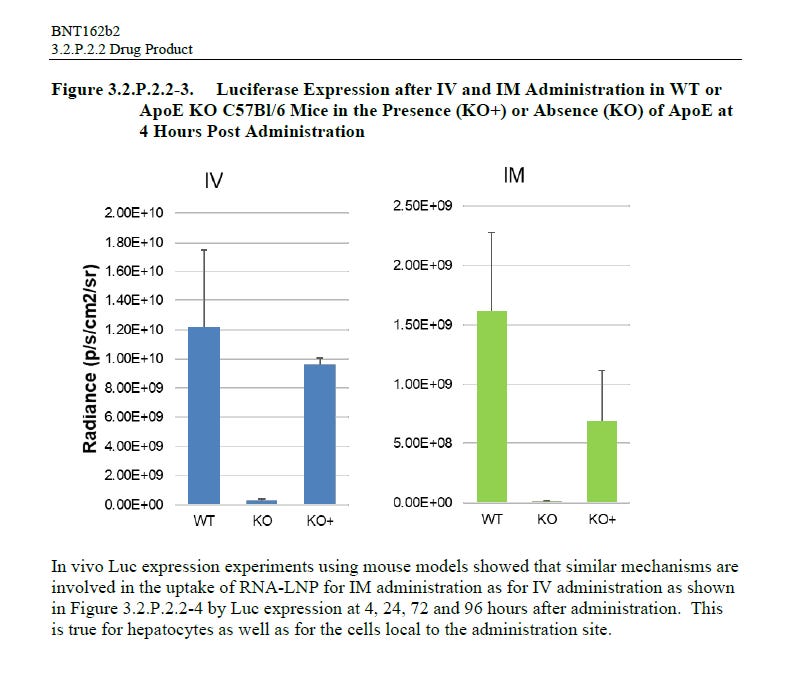
Il existe une ou deux autres études animales sur la luciférase-LNP8 entre R-20-0072 et 38166 sur le calendrier de développement non clinique impliquant des souris knock-out ApoE, qui sont résumées dans l’annexe sur le produit pharmaceutique.
Une autre information très intéressante issue de la fuite de l’EMA (rapport de qualité p56) est une autre indication concernant les différences entre BNT162b2v8 et v9 : une note de bas de page dans un diagramme indique que « RBP020.1 et RBP020.2 codent pour le même antigène, mais avec des variations ». dans les codons utilisés, ils diffèrent donc légèrement par la séquence nucléotidique. L’optimisation des codons a été réalisée soit via un algorithme propriétaire de BioNTech (RBP020.1), soit avec un algorithme publié (Raab et al. 2010 ; RBP020.2).

RBP020.1 est b2 v8, RBP020.2 est b2 v9, qui a fini par être Comirnaty. La v9 a suscité 3 à 5 fois plus d’anticorps que la v8. BioNTech doit être nul si son optimisation exclusive des codons est complètement détruite par un programme open source. Des manigances absolues quand on y pense : ils ont exploité leur propre « incompétence » pour introduire un modRNA bien optimisé en codons chez l’homme sans étude toxicologique préalable ; 38166 ont utilisé le BNT162b2v8, et l’étude de toxicité à doses répétées pour le BNT162b2v9, 20256434 , a débuté le jour même du début de l’administration de phase 3 du C4591001. Ont-ils volontairement optimisé les codons de BNT162b2v8 de manière « erronée », afin que la séquence optimale consensuelle soit bien meilleure et évite la file d’attente vers les essais sur l’homme ?
Je ne suis toujours pas entièrement sûr du triangle amoureux des brevets Genevant/Arbutus/Acuitas. Peut-être que BioNTech a eu un avant-goût des formulations ALC dans le cadre de sa collaboration avec Genevant et a décidé d’aller directement à la source ? C’est pourquoi Vivek Ramaswamy les poursuit, je pense. La collaboration contre la grippe de juillet 2018 avec Pfizer semble indiquer que Pfizer pouvait sentir une aubaine imminente, mais BioNTech leur a joué un rôle rapide et les a forcés à négocier un nouvel accord en mars 2020. Tout cela est purement spéculatif, bien sûr.
Il y a aussi la question du transfert de technologie vers Polymun et Dermapharm depuis Acuitas, qui devait être terminé à temps pour les certificats d’analyse anachroniques du 26 mars en 38166, mais cela fera l’objet d’un autre article.

et qui c’est y qui avaent ENCORE raison, hein, j’vous l’dmande ! sacrés complostistes ! pour l’instant, ont ils été pris en défaut ??????
J’aimeAimé par 2 personnes
Ça semblait évident puisque les flacons eux aussi avaient été commandés très tôt!
J’aimeAimé par 1 personne
Mais combien vont être punis?Combien vont aller en prison jusqu’à la fin de leurs jours?
J’aimeAimé par 1 personne
Combien vont être punis?Combien vont aller en prison à vie?
J’aimeJ’aime
Sur ce coup, je dois avouer que je n’a pas tout compris. En quoi, ces documents sont-ils des preuves ? La luciférase est une protéine utilisée par des insectes pour la bioluminescence.
Quand aux nano-particules, il y avait déjà eu des essais d’encapsulation d’ARNm.
En quoi cela démontre.il que le vaccin a été créé avant ?
A moins que j’aie mal compris. Je fais toujours très attention car un seul faux pas peut griller notre crédibilité quand nous utilisons des références.
J’aimeJ’aime
Regardez a quelle date Bill Gates a investi dans Moderna.
J’aimeAimé par 1 personne
Etrange nom que Luciferase ! 🤔 bon, vient de luciole mais alors pourquoi luciferase ?
J’aimeJ’aime
Probablement car il est question de luminescence, donc de lumière d’où, sans doute, le nom.
Voir en étymologie: lux, lumen (unités de mesures lumineuse), luminosité, luciole, « Lucy in the sky » (!), Lucifer ( ange déchu porteur de lumière) etc. etc.
J’aimeJ’aime
Ping: Un document déclassifié par la justice démontre que le vaccin Pfizer a été lancé en réalité en… mai 2019 sept mois avant l’apparition officielle de la covid – ANNE BELLA INFOS SANS LANGUE DE BOIS